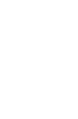高危型人乳头瘤病毒(HR-HPV)持续感染是子宫颈癌前病变及子宫颈癌发生的主要病因。子宫颈鳞状上皮内病变分为低级别鳞状上皮内病变(LSIL,即CIN 1)和高级别鳞状上皮内病变(HSIL,含CIN 2、CIN 3)。传统上,子宫颈活检确诊的CIN 2被视为切除性治疗的界定指征,而近十余年多项研究证实,CIN 2在24个月内的自然消退率较高,尤其30岁以下女性,其进展为浸润癌的风险低于0.5%;但长期保守观察下,CIN 2女性进展为浸润癌的风险会再次升高。因此,CIN 2临床处理的核心是实现精准化管理,明确保守观察与治疗的适应证、监测随访策略及特殊人群的管理方案,成为临床亟需解决的问题。中国优生科学协会阴道镜和宫颈病理学分会与中华医学会妇科肿瘤学分会联合组织专家,依据循证医学原则、结合中国国情制定本共识,旨在指导临床开展CIN 2的个体化、精细化规范管理。
一、CIN 2的流行病学和自然史
01 CIN 2发病率
目前全球尚无CIN 2统一的登记统计数据。英国一项针对未接种HPV疫苗女性的子宫颈癌筛查研究显示,每年约2%~3%的女性被诊断为CIN 2/CIN 3,其中25~29岁年龄段发病率最高,可达10%;我国组织病理学确诊的CIN 2、CIN 3及以上病变的世标发病率分别为1.3%和1.2%。
02 CIN 2自然转归率
国外多篇文献报道,对CIN 2女性随访2年,50%~60%的病变可自然消退为CIN 1或正常宫颈组织,23%~32%的病变持续存在,18%~23%的病变发生进展;其中<30岁女性的病变消退率可达60%。我国研究显示,生育年龄CIN 2患者随访3~66个月,63%~78.6%的病变消退,9.2%~22%的病变持续存在,12.2%~15%的病变进展至CIN 3,且所有研究对象均未发现进展为子宫颈癌的情况。
二、CIN 2的阴道镜和组织病理学表现
01 CIN 2的阴道镜下表现
CIN 2的阴道镜诊断与组织学诊断难以达到较高的符合度,其各项特征均介于CIN 1与CIN 3之间,具体表现如下:
①位置:多数病变位于子宫颈转化区,紧邻鳞柱交接部(SCJ),有时表现为孤立的病变(图1A),也可能混杂于大面积病变中(图1B);
②颜色:醋酸作用后,醋白改变较CIN 1更不透亮,且持续时间更长,但致密性和持续时间均不及CIN 3;
③轮廓:病变常表现为斑片状、轻度增厚,无法仅通过轮廓与CIN 1、CIN 3准确鉴别;
④边界:边界形态往往缺乏CIN 1典型的不规则或地图样改变;
⑤血管征象:若存在血管征象,多为细小到中等管径,显著程度低于CIN 3,血管间距与CIN 1相近或稍大,少数情况下接近CIN 3(图1C);若见非典型血管,需警惕浸润性子宫颈癌与高级别病变共存的可能;
⑥碘染色:病变多呈碘不染色(图1D),少数情况下也可能出现黄棕色部分碘染表现。
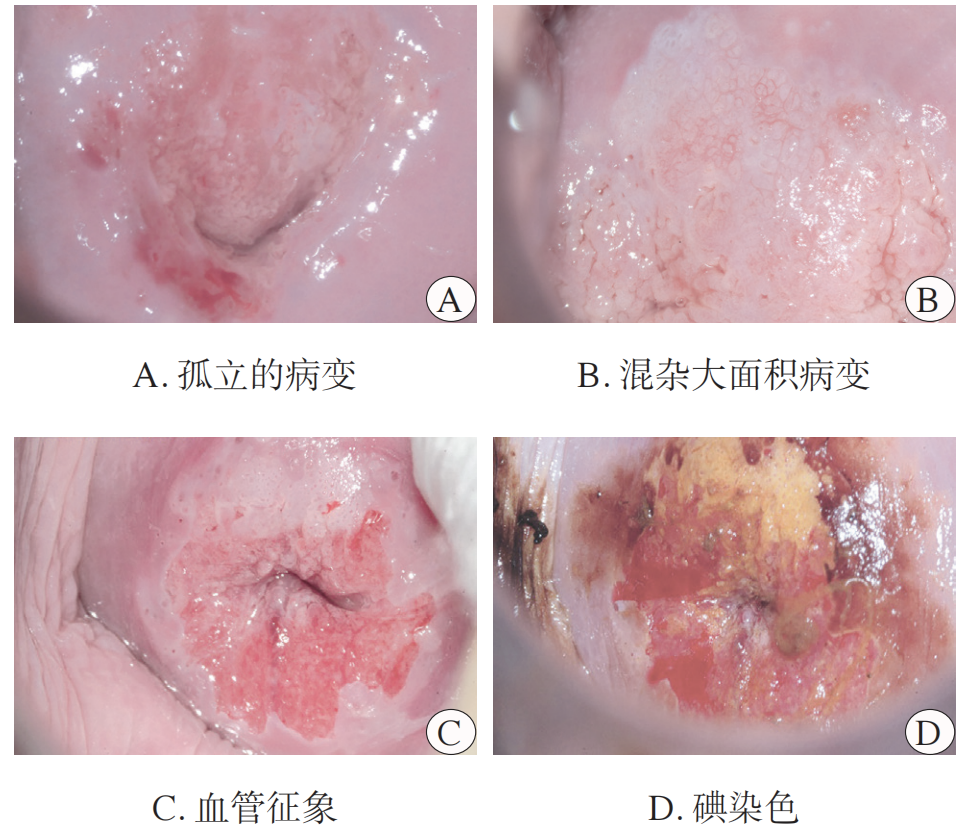
图1:CIN 2的阴道镜图像
另外,需特别关注薄型HSIL(组织学上皮细胞层厚度<10个),此类病变阴道镜下多为小灶病变,91.6%易被判定为低级别印象,且83.3%的组织病理学类型为CIN 2,因此阴道镜下活检时,无论镜下印象为化生或更高级别异常,均需在醋白上皮区域行多点活检。
子宫颈管搔刮(endocervical curettage, ECC)相关研究显示:在阴道镜评估为低级别病变、伴3型转化区的女性中,ECC在细胞学低度异常[未明确诊断意义的不典型鳞状细胞(ASC-US)/低级别鳞状上皮内病变(LSIL)]人群中未检出CIN 2及以上病变(CIN 2+);细胞学高度异常[不能排除高级别鳞状上皮内病变的不典型鳞状细胞(ASC-H)及以上]是ECC检出CIN 2+的唯一独立因素;ECC对阴道镜活检漏诊CIN 2+的诊断增益为2.9%。多因素分析提示,HPV 16阳性与ECC的额外诊断获益存在独立关联。目前尚无充分证据支持对CIN 2患者常规行ECC,但对于3型转化区、病变向颈管内延伸、细胞学高度异常,以及HPV 16/18持续感染人群,应重视ECC检查并做好精准评估。
02 CIN 2的组织病理学表现
CIN 2的病理形态介于CIN 1与CIN 3之间,兼具两者部分特征,病理医师间的诊断一致性相对较低。其核心表现为鳞状上皮细胞异型性、核浆比增高,可见核分裂象,偶见病理性核分裂象,异常细胞多分布于上皮层上1/2及以下区域。CIN 2与CIN 3的关键区别在于,病变上皮仍保留部分分化特征,尤其中表层细胞可见中间型细胞及表层鳞状上皮的分化表现;中表层常可见HPV感染相关的挖空细胞,这一点与CIN 1相似。但CIN 2的细胞增殖活性及异型性均高于CIN 1,表现为基底及副基底层细胞核浆比增高,核分裂象更易见,且可出现于上皮中层(图2A,B)。此外,CIN 2需与非HPV感染相关的上皮增生、化生性病变相鉴别,如不成熟鳞状上皮化生、移行上皮化生、炎症反应性增生等。免疫组化对CIN 2诊断具有辅助价值:绝大多数CIN 2呈p16大片状强阳性,仅少数HPV非依赖型HSIL可表现为p16阴性。需注意的是,20%~40%的CIN 1亦可出现p16阳性,因此不可仅凭p16阳性诊断CIN 2,需结合形态学特征与HPV状态综合判断。Ki-67增殖指数方面,CIN 2的阳性细胞可延伸至上皮中上层,阳性比例显著高于CIN 1,但目前尚无统一诊断阈值(图2C,D)。现有研究表明,上述免疫标志物对CIN 2的消退或进展无明确预测意义,临床处理仍需结合临床表现、患者年龄等因素综合决策。
图2: CIN 2的HE和免疫组化染色
应规范CIN 2的病理诊断描述:标注送检标本类型(活检或锥切),诊断应注明:高级别鳞状上皮内病变/子宫颈上皮内瘤变2级(HSIL/CIN 2);必要时进行p16和Ki-67免疫组化染色,描述包括p16染色模式,Ki-67染色百分比及阳性信号所在部位。
三、CIN 2的保守观察
对于经阴道镜活检病理确诊的CIN 2患者,需精准区分两类人群:一类为高风险人群,即存在CIN 3+漏诊可能,或CIN 2持续存在、进展为CIN 3+风险较高者,可通过宫颈切除性治疗明确诊断并从中获益;另一类为低风险人群,即上述风险较低者,可采取保守观察策略,通过密切监测与动态评估,最大限度避免即刻有创治疗。相关评估因素包括患者年龄、生育需求、宫颈细胞学结果、HPV型别、阴道镜下鳞柱交界(SCJ)可见性、病变特征及机体免疫功能状态等。
(一) CIN 2保守观察的主要决定因素
1.年龄:年龄是预测CIN 2消退或进展的核心因素之一。年轻女性,尤其是<25岁者,处于性活跃阶段,HPV感染率相对较高,但机体免疫系统更为活跃、免疫应答能力更强,HPV感染多呈一过性。研究显示,<25岁的CIN 2患者中,88%的病变可自然消退,平均消退时间为21个月。我国本土研究数据也提示,<25岁患者的HSIL消退率显著高于≥25岁者,病变消退时间(12个月vs15个月)亦更短。而≥30岁女性经长期随访,进展为浸润癌的风险更高,该人群若选择保守观察,需采取更严密的监测与评估。
2.HR-HPV型别:研究显示,HR-HPV阳性者CIN 2进展风险(25%)显著高于阴性者(3%);其中以HPV 16阳性进展风险最高(71%),其次为HPV 18(48%)。HPV 16阳性的CIN 2患者经24个月保守观察后,47%进展至CIN 3+。多因素分析提示,HPV 16阳性可使病变进展风险升高1.97~4.8倍。
3.细胞学异常:细胞学高度异常(ASC-H及以上)的CIN 2患者,病变进展风险高达25%~60%;其中细胞学为HSIL者,阴道镜下漏诊CIN 3+、病变持续或进展的风险升高3.8~5.0倍。此外,细胞学HSIL或HPV 16阳性的CIN 2患者,其病变消退时间是细胞学低度异常(ASC-US/LSIL)或非HPV 16阳性者的2~3倍;但中位随访25个月期间,所有患者均未发现宫颈癌。
4.阴道镜下SCJ可见性:阴道镜下鳞柱交界(SCJ)是否可见,是CIN 2保守管理决策的关键参考因素。研究显示,与SCJ可见者相比,SCJ不可见者的宫颈癌漏诊风险分别为0.6%和0.3%(P=0.011)。我国本土研究亦提示,在CIN 2患者中,SCJ不可见时病变漏诊风险可升高9.6倍。
5.CIN 2病变特征:国内一项研究显示,多象限受累的CIN 2病变消退率(42%)低于单象限受累者(80%),而进展率更高(27%vs6%)。国外研究亦表明,对CIN 2女性随访3个月发现,病变受累范围是影响消退的重要因素,局限于1个象限的病变消退率显著高于多象限受累者。此外,若高级别病变广泛累及宫颈腺体隐窝、呈扩张性CIN(expansile CIN)表现,可能升高疾病进展风险,临床决策时需谨慎评估。
➱推荐意见
①<25岁CIN 2女性:优先推荐保守观察,治疗亦可作为可接受的备选方案;
②≥25岁有生育需求女性(若对切除性治疗可能影响后续妊娠的顾虑,超过对病变进展风险的担忧),在SCJ及病变上界可见、宫颈管未检出CIN 2、无宫颈病变治疗史,且具备规范随访条件时,可选择保守观察;
③对病变范围广泛(累及>2个象限)、扩张性CIN、HPV 16/18持续阳性、细胞学提示高度异常(ASC-H、不典型腺细胞AGC、HSIL)等病变持续/进展高风险者,保守观察应格外慎重。
(二)CIN 2保守观察流程及监测
对于计划实施保守观察的CIN 2女性,需首先全面评估其病史、细胞学检查、阴道镜印象及活检病理结果,明确除外腺上皮病变及可疑浸润癌。临床需充分告知患者保守观察的管理目标、阴道镜检查的局限性(如病变漏诊风险)、病变持续或进展的可能性,以及延迟治疗可能带来的相关风险,同时明确要求其严格按时随访,并签署知情同意书。保守观察具体流程详见图3。

图3:CIN 2保守观察管理流程
1. 保守观察的常规监测:需按年龄分层开展监测,<25岁者行细胞学检查;≥25岁者采用以HPV为基础的检测(单独HPV检测或HPV联合细胞学检测),同时配合阴道镜评估。对阴道镜下所有不连续醋白上皮区域(无论提示为化生或更高级别异常),均应行定位活检±宫颈管搔刮(ECC)。宫颈活检虽具有一定促进病变消退的作用,但仍需警惕CIN 2进展风险,坚持对病变进行动态监测。
2. 保守观察的新型监测标志物:①甲基化检测:研究显示,甲基化检测阳性联合细胞学高度异常可预测CIN 2进展;其中FAM19A4/miR124-2甲基化阴性者病变临床消退率(74.7%)显著高于阳性者(51.4%)。② HR-HPV基因整合:研究表明,HR-HPV整合阳性组进展为HSIL的风险是阴性组的5.6倍;一项针对HR-HPV整合与CIN 2/3自然转归的在研研究显示,整合阳性组CIN 2持续/进展率为58.82%,显著高于阴性组(15.29%)。上述标志物目前均处于临床研究阶段,尚需更多大样本研究数据予以证实。
3. 终止保守观察的指征:①若检出CIN 3及以上病变(CIN 3+),或CIN 2病变持续存在满2年,应行宫颈切除性治疗;②病变范围扩大、延伸至宫颈管内,或阴道镜下无法观察病变上界、SCJ不可见时,需及时终止保守观察。
4. CIN 2降级后随访方案:连续2次检测(间隔6个月)满足细胞学<ASC-H,或HPV阴性且阴道镜活检病理<CIN 2,后续按年龄分层每年检测1次;若结果均为阴性,可继续每年随访1次并持续2年,此后改为每3年随访1次,总随访时长至少25年。
四、CIN 2的治疗
CIN 2的主要治疗方式分为两类:①保守性治疗:包括消融治疗(激光、冷冻、热凝、电凝等)及光动力治疗等;②子宫颈切除性治疗:主要术式为环形电切术(loop electrosurgical excision procedure, LEEP)和冷刀锥切术(cold knife conization, CKC)。
(一)消融治疗
消融治疗具有操作简便、无需麻醉或仅需局部麻醉、术后恢复快等优势,但无法获取组织学标本,不能开展病理学评估。研究显示,CO₂激光消融与LEEP的临床疗效及妊娠结局均无显著差异,宫颈冷冻、热凝治疗同样是CIN 2的有效治疗手段。一项系统综述显示,HSIL患者接受消融术(冷冻、热凝、激光)后,病变持续/复发风险显著高于切除性治疗(RR=1.65,95%CI 1.25~2.19;随访12个月时RR=1.78,95%CI 1.27~2.51),二者安全性相当。因此需在全面排除浸润癌和腺上皮病变风险后,谨慎选择消融治疗。
消融治疗适应证:①SCJ和病灶完全可见;②宫颈管内无组织学证实的高级别上皮内病变;③全部病变均在可治疗范围内。治疗前需排除浸润癌可能。若病灶范围超过宫颈表面积75%、病变向颈管内延伸、合并腺上皮病变、有HSIL治疗史,以及处于妊娠期、急性炎症期,均不适宜行消融治疗。
消融治疗注意事项:①术前需再次评估病史、细胞学结果、阴道镜印象、组织病理及治疗适应证,签署知情同意书;②治疗宜在月经干净后进行,术前3天避免性生活、阴道冲洗及用药;③可采用宫颈局部麻醉(宫颈内阻滞或宫颈旁阻滞);④术中密切观察患者反应,部分患者可出现短暂迷走神经兴奋症状,如脸红、头晕、头痛等,多数患者伴轻微下腹坠痛,一般可自行缓解;⑤术后可出现不同程度阴道排液,多在10~20天缓解;若出现发热、异常出血或严重盆腔疼痛,应及时复诊。术后1个月禁止性生活、游泳及盆浴,通常无需常规使用抗生素,既往有盆腔炎者可酌情预防用药。治疗后需按常规定期随访。
(二)光动力治疗
光动力疗法(photodynamic therapy, PDT)是一种依托光敏剂、特定波长光源与组织内氧分子协同作用的药械结合靶向治疗技术。其主要优势在于对宫颈结构损伤小,对流产、早产等不良妊娠结局影响较轻,适用于年轻、有生育需求的女性。
根据给药途径与光敏剂不同,目前临床常用的PDT主要有三类:①5-氨基酮戊酸光动力疗法(ALA-PDT):国内一项前瞻性队列研究显示,ALA-PDT治疗CIN 2患者,6个月病变消退率可达92%。②血卟啉注射液光动力疗法(HpD-PDT):国内一项小样本研究显示,经HpD-PDT治疗并随访12个月,CIN 2、CIN 3病变消退率分别为100%和84.2%,但治疗后需严格避光。③氨酮戊酸己酯光动力疗法(HAL-PDT):采用光敏剂与阴道内冷光源一体化自动装置。一项全球多中心、随机双盲安慰剂对照研究显示,经1~2次HAL-PDT治疗后,CIN 2患者病变消退率为95%。
PDT适应证:年轻、有生育需求的女性;宫颈SCJ及病变上界完全可见;无宫颈管内HSIL;无浸润癌及腺上皮病变。病变范围较大者需慎重选择。推荐使用经国内外权威机构认可、临床试验证实可用于CIN 2治疗的PDT方案。
禁忌证:细胞学或组织学提示腺上皮病变、浸润癌,或临床高度怀疑恶性病变者;对红光等相关光源过敏者;卟啉症患者或对ALA、凝胶及制剂成分过敏者;妊娠及哺乳期女性。
目前PDT治疗CIN 2的证据多来自小样本研究及少量随机对照试验,其长期安全性以及与切除性治疗的对比数据,仍有待更多高质量研究进一步验证。
(三)切除性治疗
子宫颈切除性治疗主要可选择环形电切术(LEEP)或冷刀锥切术(CKC),二者临床疗效及术后病变残留、复发风险相当。但为减少手术对未来妊娠的不利影响,有生育需求的CIN 2女性建议优先选择LEEP;若筛查结果、阴道镜印象或组织病理学结果不除外子宫颈浸润癌,可根据情况选择CKC术。
多项研究证实,子宫颈切除性治疗可能增加早产、胎膜早破、低出生体重儿等不良妊娠结局,且不良妊娠风险与宫颈组织切除深度呈正相关。研究显示,早产风险随切除深度增加而升高,切除深度每增加1mm,早产风险约增加6%;瑞典一项研究亦发现,切除深度在3~10mm之间时,早产风险无明显差异,超过10mm后,每增加1mm,早产风险增加15%。宫颈切除深度需以完整覆盖病变上界及转化区为核心原则,同时兼顾生育需求:研究表明,<30岁女性中1型/2型转化区占比达85.7%,因此该年龄段CIN 2女性,采用约10mm的切除深度,通常可在保证治疗效果的同时,最大限度降低对未来妊娠的不利影响,具体仍需结合个体宫颈解剖特点灵活调整。
子宫颈切除性治疗适应证:随访观察期间任一节点检出CIN 3+;随访观察满2年CIN 2未自然消退;病变范围扩大、延伸至宫颈管内,或阴道镜下无法观察病变上界、SCJ不可见;治疗后复发的CIN 2;以及因担心肿瘤进展风险,不愿接受随访观察的患者。
子宫颈切除性治疗后妊娠时机:研究显示,LEEP术后6个月、CKC术后9个月,宫颈组织可修复至术前90%的长度。临床数据提示,宫颈切除性治疗后至妊娠时间<14个月,早产风险升高;<15个月,胎膜早破风险升高;国内一项研究进一步证实,术后<12个月妊娠,或妊娠中期宫颈长度<25mm,是预测胎膜早破和早产的独立危险因素。因此,建议宫颈切除性治疗后6~12个月再计划备孕,妊娠期需动态监测宫颈管长度;不建议常规行预防性宫颈环扎术,以避免对宫颈造成二次损伤。
➱推荐意见
①CIN 2女性选择保守性治疗需格外慎重,其适应证至少应满足:转化区及病灶完全可见,且需充分排除浸润癌、腺上皮病变的相关风险。
②对于有生育需求的CIN 2女性,切除性治疗优先推荐LEEP术,术中需严格把控切除深度,在确保完整切除病变组织的基础上,最大限度降低对未来妊娠的不利影响。
五、特殊人群CIN 2的管理
01妊娠合并CIN 2的管理策略
妊娠期女性免疫系统与生理机能均处于特殊状态。目前尚无证据表明,妊娠本身会加速子宫颈癌前病变进展,亦无证据显示妊娠期上皮内病变会影响妊娠结局。对于经组织学确诊的妊娠合并CIN 2,临床以随访观察为主;分娩方式需严格依据产科指征决定,CIN 2并非选择性剖宫产的指征。
当妊娠期出现非产科因素阴道出血、同房后出血;肉眼观察宫颈外观异常、盆腔检查明显异常;或宫颈癌筛查结果异常时,均需转诊至阴道镜检查。妊娠期阴道镜检查的核心目的是排查子宫颈癌,检查时间无严格限制,但因妊娠晚期宫颈暴露困难,优先选择妊娠早中期进行;需注意,妊娠期禁止行宫颈管搔刮(ECC)。
妊娠期阴道镜检查建议由经验丰富的医师操作,操作流程与非妊娠期一致。术前需与患者充分沟通,明确告知检查目的、风险及注意事项,获得知情同意后再行操作,并做好活检及出血应急处理准备。对于3%~5%醋酸涂抹后已呈现典型高级别病变特征的部位,复方碘染色可无需常规进行;若可疑存在高级别病变或更严重病变,需行宫颈活检,推荐采用微量活检钳,在病变最明显部位取样。若阴道镜检查后出现出血量多、腹痛等异常情况,需及时就医就诊。
对于经宫颈活检组织学确诊为CIN 2的妊娠期患者,建议每间隔12周左右复查宫颈细胞学及阴道镜检查,持续至妊娠晚期;产后6周需再次全面评估宫颈细胞学及阴道镜情况。若复查时细胞学提示可疑浸润癌,或阴道镜下观察到宫颈局部病变进展,推荐重复宫颈活检,进一步明确病变性质及程度。
02绝经后女性CIN 2的管理策略
绝经后女性因雌激素缺乏,可出现下生殖道萎缩、病变多隐匿于宫颈管内、宫颈管搔刮(ECC)敏感性降低等情况,导致阴道镜下活检漏诊CIN 2+的风险显著升高。研究显示,≥45岁女性中,CIN 2+漏诊率达54.5%,行LEEP术后进一步检出CIN 2+的风险增加17.7%。国内研究亦提示,≥50岁、组织学提示LSIL且持续2年及以上的患者,行宫颈锥切术后,病理升级为HSIL的比例达34.56%,其中CIN 2占11.76%、CIN 3占22.79%,充分说明绝经后女性阴道镜检查对高级别病变的漏诊风险较高。此外,绝经后女性还需高度警惕子宫颈癌的漏诊,国内一项研究表明,≥50岁经阴道镜活检诊断为宫颈HSIL的患者,行宫颈切除性治疗后,最终确诊为子宫颈浸润癌的比例达11.5%。
鉴于绝经后女性阴道镜诊断准确性下降,高级别病变及浸润癌漏诊风险显著增高,在充分评估患者身体状况、排除手术禁忌证的前提下,绝经后CIN 2女性首选宫颈切除性治疗。无相关禁忌证时,可在治疗前给予1~2周局部雌激素制剂预处理,以改善下生殖道萎缩状态,提高手术安全性及疗效。全子宫切除术不作为CIN 2的首选治疗方案,仅在以下情况可考虑选用:HSIL病灶残留、下生殖道严重萎缩导致重复宫颈切除性手术难度大、HSIL合并其他需手术治疗的妇科疾病,以及术后无法配合随访或随访依从性极差的患者。
03免疫功能低下人群CIN 2的管理策略
因感染人类免疫缺陷病毒(HIV)导致的免疫抑制患者,或自身免疫性疾病(如系统性红斑狼疮、风湿性关节炎等)需长期服用免疫抑制剂的患者,其HPV持续感染风险、病变进展风险及治疗失败风险均会显著升高。尽管抗逆转录病毒药物治疗HIV可能在一定程度上提高CIN病变的消退概率,但目前针对此类人群的相关研究证据仍较有限。因此,该人群采用保守观察策略需格外慎重,需综合考量疾病自身风险与免疫功能状态对治疗效果及预后的影响,核心管理原则为个体化评估、强化监测或积极干预,确保治疗方案与患者免疫状态、疾病风险相适配。
➱推荐意见
①妊娠期CIN 2女性:需先排除浸润癌,遵循以随访观察为主、产后重新评估的管理原则;
②绝经后CIN 2女性:首选子宫颈切除性治疗;
③免疫功能低下CIN 2女性:采用个体化评估、强化监测或积极干预的策略。
六、CIN 2治疗后的管理
对CIN 2患者的长期随访队列研究显示,保守观察组与切除性治疗组在2年内的子宫颈浸润癌累积风险无显著差异。但随访延长至20年时,保守观察组的浸润癌累积风险明显高于切除性治疗组,该差异在≥30岁女性中更为显著。因此,无论CIN 2患者选择何种治疗方式,术后长期规范随访均至关重要,是及时发现病变残留、复发及进展,降低浸润癌风险的关键。
01CIN 2治疗后的随访管理
对于具备长期随访条件的患者,推荐术后6个月行以HPV为基础的检测(单独HPV检测或HPV联合细胞学检测)。若检测结果为阳性,需进一步行阴道镜检查,明确有无病变残留或复发;若检测结果为阴性,推荐后续每12个月行1次以HPV为基础的检测。当连续3次检测均为阴性后,可调整随访间隔为每3年1次,总随访时长需持续至少25年。对于年龄超过65岁、已完成25年规范随访,且健康状况允许的患者,可继续维持每3年1次的随访频率,持续监测病情变化。需重点注意,无论随访阶段如何,只要HPV检测结果为阳性,均需及时行阴道镜检查评估。
02CIN 2治疗后的健康教育
告知患者CIN 2治疗后5年内复发风险约5%~10%,强调规范长期随访的重要性;性生活全程使用避孕套可显著提升CIN 2消退率(53%vs35%)与HPV清除率(23%vs9%);建议<45岁女性接种预防性HPV疫苗。意大利一项前瞻性研究显示,术后4年未接种疫苗组临床复发率为6.4%,接种疫苗组仅1.2%,复发风险显著降低81.2%。同时鼓励患者戒烟、保持规律运动。此外,临床研究显示约40%的患者会出现焦虑情绪,应根据需求提供专业的心理咨询与支持。
➱推荐意见
CIN 2治疗后推荐采用以HPV检测为基础的随访方案,定期随访至少25年。需综合患者年龄、生育需求、HPV感染状态、治疗方式、手术切缘及随访依从性等因素进行个体化管理,同时强化规范随访、鼓励接种预防性HPV疫苗,并加强健康教育。
总之,CIN 2是一类生物学异质性显著的中度宫颈上皮内病变,临床风险介于CIN 1与CIN 3之间:既不同于多数可自然消退的CIN 1,也不同于进展风险更高的CIN 3。因此,CIN 2的管理核心并非“一刀切式治疗或单纯观察”,而应精准识别不同风险人群,实施个体化、精细化管理。在保护有生育需求女性、减少切除性治疗不良影响的同时,避免因保守观察不当造成高级别病变漏诊,在兼顾生育需求的前提下,最大程度降低病变漏诊与进展风险。
图文来源:中国妇产科临床杂志,2026,27(01):89-96.
责编:霍盼