卵巢癌是妇科恶性肿瘤中病死率最高的类型之一,其5年生存率长期维持在40%左右。近年来,多腺苷二磷酸核糖聚合酶(poly ADP ribose polymerase,PARP)抑制剂的问世彻底改变了卵巢癌的治疗模式,为患者带来了显著生存获益。目前,PARP抑制剂已在我国临床广泛应用,为进一步规范此类药物的临床应用,中华医学会妇科肿瘤学分会先后制定《卵巢癌PARP抑制剂临床应用指南》2020版及2022版。随着临床研究数据的持续更新及临床实践经验的逐步积累,亟需对指南进行修订完善,经中华医学会妇科肿瘤学分会编写组专家充分讨论、投票表决,最终形成《卵巢癌PARP抑制剂临床应用指南(2025版)》(以下简称“本指南”)。
本指南采用中华医学会妇科肿瘤学分会临床诊疗指南推荐类别,见表1。

本指南中,卵巢癌包括输卵管癌和原发性腹膜癌。本指南不涉及国内未上市的PARP抑制剂。本指南临床研究中乳腺癌易感基因(breast cancer susceptibility gene,BRCA)突变为致病性或可能致病性突变。
PART 01 PARP抑制剂及其作用机制
1963年,Chambon等首次发现聚腺苷二磷酸核糖聚合酶(PARP),后续研究证实其参与DNA单链损伤后的修复过程。1980年,Durkacz等证实烟酰胺类似物可抑制PARP的修复功能,同时能够增强DNA损伤剂硫酸二甲酯的细胞毒性,提示这类化合物有望作为增敏剂,与细胞毒性药物联合用于肿瘤治疗。2005年,《自然》(Nature)同期发表的两项研究,首次证实PARP抑制剂与BRCA1/2基因突变之间存在“合成致死”效应。目前已知,PARP家族包含17个成员,其中PARP1与PARP2主要通过碱基切除修复(base excision repair,BER)途径,在DNA单链断裂(single strand break,SSB)的修复过程中发挥关键作用。
PARP抑制剂历经三代迭代更新,第三代PARP抑制剂以复合物单晶结构为研发基础,具备活性高、选择性强等显著优势。
多项临床研究证实,晚期卵巢上皮性癌患者接受PARP抑制剂维持治疗,可获得显著临床获益。
1.1作用机制
BRCA1/2基因为抑癌基因,在DNA损伤修复、维持细胞正常生长等方面发挥着关键作用。这类基因突变会削弱细胞对DNA损伤的正常修复能力,进而引发同源重组缺陷(homologous recombination deficiency,HRD)——即BRCA功能缺失,或其他同源重组相关基因发生突变、功能异常,导致DNA双链断裂无法通过同源重组修复(homologous recombinant repair,HRR)途径完成修复,最终诱发细胞癌变。
PARP则在DNA单链损伤的碱基切除修复过程中起到核心作用。在HRD肿瘤细胞中,DNA双链断裂的修复通路已存在缺陷,此时PARP抑制剂进一步阻断DNA单链的修复进程,二者共同作用形成“合成致死”效应,最终导致肿瘤细胞死亡。
PARP抑制剂对PARP的作用机制主要体现在两个方面:
(1)于PARP活性位点与烟酰胺腺嘌呤二核苷酸展开竞争,从而抑制多聚(ADP-核糖)聚合物的生成;
(2)结合至PARP1和(或)PARP2的烟酰胺腺嘌呤二核苷酸结合口袋,促使其发生构象异构,阻碍DNA与PARP的可逆解离,使PARP持续结合于DNA上。这一现象被称为DNA-PARP 复合物的“捕获效应(trapping)”,会导致该复合物长期滞留,进而抑制DNA后续的修复过程。
越来越多临床研究证实,PARP抑制剂的获益人群并非局限于BRCA突变或HRD阳性的卵巢癌患者,铂敏感型卵巢癌患者同样能从中显著获益,这一效应可能与PARP抑制剂的捕获作用密切相关。
1.2药理学特性
不同PARP抑制剂的药理学特性存在一定差异,已分别获得美国食品药品监督管理局(Food and Drug Administration,FDA)与中国国家药品监督管理局(National Medical Products Administration,NMPA)批准的多款PARP抑制剂,在生物利用度、半衰期、代谢途径及组织分布等方面各具优势。
1.2.1
奥拉帕利 (olaparib)
该药物现有片剂与胶囊两种剂型,其中胶囊剂型目前尚未在中国提交上市申请。片剂经口服给药后,1.5小时可达到中位血浆浓度;体外实验显示其蛋白结合率约为82%,表观分布容积(apparent volume of distribution,Vd)为(158±136)L。该药物在体内主要通过CYP3A4/5酶通路代谢,单次给药300mg后,药物半衰期为(14.9±8.2)小时。
1.2.2尼拉帕利 (niraparib)
该药物的胶囊剂型,绝对生物利用度约为73%,口服给药后3小时内即可达到血浆峰浓度。其与人血浆蛋白的结合率为83.0%,表观分布容积(Vd)为(1220±114)L;在体内主要经羧酸酯酶代谢,先形成无活性代谢产物,后续进一步发生葡萄糖苷化反应,药物平均半衰期为36小时。
1.2.3氟唑帕利 (fluzoparib)
氟唑帕利的胶囊剂型,单次口服150mg后,2.5小时达到血浆峰浓度;人血浆蛋白结合率为74.3%~81.6%,稳态表观分布容积为(34.6±14.5)L。该剂型在体内主要通过CYP3A4酶代谢,150mg剂量多次给药后,药物的平均末端消除半衰期约为(9.14±2.38)h。
1.2.4帕米帕利 (pamiparib)
帕米帕利的胶囊剂型,口服给药后1~2小时即可达到血浆峰浓度;稳态状态下,其人血浆蛋白结合率为95.7%,且40mg剂量的暴露量与60mg接近。在有限的中国患者人群中,采用40mg每日2次的给药方案时,帕米帕利的表观分布容积(Vd)约为37L。该药物在体内主要经CYP2C8和CYP3A酶代谢,血浆消除半衰期约为13h。在临床治疗剂量下,本品不太可能对肠道外排转运蛋白P-糖蛋白(P-glycoprotein,P-gp)、乳腺肿瘤耐药蛋白(breast cancer resistance protein,BCRP),以及有机阴离子转运多肽(organic anion transporting polypeptide,OATP)1B1/1B3、肾摄取转运蛋白有机阳离子转运蛋白(organic cation transporter,OCT)2、有机阴离子转运蛋白(organic anion transporter,OAT)1与OAT3产生抑制作用。
1.2.5塞帕帕利 (senaparib)
该药物的胶囊剂型经口服给药后吸收迅速,无论是单次给药还是每日1次连续给药,血浆浓度的中位达峰时间(Tmax)均约为2小时,与人血浆蛋白的结合率为96.13%。其体内主要代谢酶为CYP3A4,且未发现人体专属代谢产物。基于群体药代动力学(PopPK)分析,以100mg剂量每日1次连续给药时,药物血浆有效半衰期的几何均值为8.92h。在临床治疗剂量下,本品不太可能对肠道外排转运蛋白P-糖蛋白(P-gp)、乳腺肿瘤耐药蛋白(BCRP),以及有机阴离子转运多肽(OATP)1B1/1B3、有机阳离子转运蛋白(OCT)3、有机阴离子转运蛋白(OAT)产生抑制作用;同时,本品也不大可能成为BCRP、OATP、OAT、OCT类转运体的底物。
1.3获批情况
目前美国FDA批准4种PARP抑制剂、中国NMPA批准5种PARP抑制剂应用于临床,其适应证见表2。

1.4应用PARP抑制剂的生物标志物
BRCA基因突变或HRD是目前常用的PARP抑制剂应用生物标志物。
1.4.1BRCA基因检测
BRCA基因突变是PARP抑制剂敏感性首选的生物标志物。该基因突变主要分为胚系BRCA(germ line BRCA,gBRCA)突变与体细胞BRCA(somatic BRCA,sBRCA)突变两类,而从肿瘤组织样本中检测到的BRCA突变,则统一以组织细胞BRCA(tissue BRCA,tBRCA)突变进行表述。目前国内外多采用二代测序(next-generation sequencing,NGS)技术开展检测,常见突变类型涵盖点突变、小片段插入或缺失等。针对胚系变异的BRCA基因检测报告解读,需参照国际癌症研究机构(International Agency for Research on Cancer,IARC)制定的分类标准执行(见表3)。
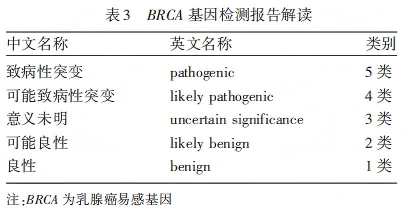
本指南推荐卵巢癌患者在初次病理确诊时即进行BRCA基因检测。
1.4.2HRD检测
除BRCA1/2基因突变外,RAD51、ATM、PALB2、MRE11等其他同源重组修复(HRR)相关基因发生损伤或功能缺失,同样会引发同源重组缺陷(HRD),而HRD作为PARP抑制剂敏感性的生物标志物,目前已正式应用于临床实践。HRD 检测的应用,能够将PARP抑制剂的敏感人群从约占25%的BRCA突变群体,拓展至约占50%的HRD阳性群体。HRD的判定主要可通过同源重组相关基因突变检测与基因瘢痕检测两种策略实现。前者是在基因水平借助二代测序(NGS)平台,对同源重组相关基因开展全面检测,但该方法存在一定局限性:
(1)除BRCA基因外,其余HRR相关基因的检出率普遍偏低;
(2)不同检测方案纳入的HRR相关基因存在差异,尚无公认的统一标准;
(3)无论是HRR基因突变检测还是HRD基因瘢痕检测,均无法有效识别同源重组通路基因的表观遗传改变(如BRCA1启动子区甲基化),故而存在一定的假阴性率;
(4)不同基因对同源重组通路功能的影响程度存在差异,且缺乏统一的量化评估指标;
(5)检测的经济成本效益需纳入考量,并向受检者充分知情告知。
目前在PARP抑制剂相关临床试验中,HRD检测多采用基因瘢痕检测法,该方法不仅能够明确BRCA基因的突变状态,还可对基因的不稳定性类型进行综合分析。
目前国际上已有两款技术较为成熟的HRD检测平台,分别为Myriad myChoice® CDx(Myriad Genetic Laboratories, Inc.)与FoundationFocus™ CDx BRCA LOH(Foundation Medicine, Inc.)。
FoundationFocus™ CDx BRCA LOH检测主要包含两项核心指标:肿瘤BRCA(tBRCA)突变状态及基因组杂合性缺失(loss of heterozygosity,LOH)。其判定标准为:若检出tBRCA突变,无论LOH比率高低,均判定为HRD阳性;若tBRCA无突变,但LOH比率≥16%,同样归为HRD阳性;若BRCA为野生型且LOH比率<16%,则定义为HRD阴性。
Myriad myChoice® CDx检测则通过综合评估肿瘤样本中与基因组不稳定性相关的三项指标进行判定,即杂合性缺失(LOH)、端粒等位基因不平衡(telomeric allelic imbalance,TAI)及大片段迁移(large-scale transition,LST)。具体判定规则为:评分≥42分,或检出BRCA1/2突变,均判定为HRD阳性;评分<42分且BRCA为野生型,则判定为HRD阴性。
需要指出的是,上述两款检测平台均缺乏基于中国人群的大样本前瞻性临床研究验证,HRD检测方案的设计需充分结合我国人群的分子遗传学特征。目前国内HRD检测产品尚未正式获批上市,但已有研究团队基于中国人群的遗传多态性数据开展HRD算法的开发工作,相关检测平台已应用于部分临床研究。其中,基于ADx-GSS算法的HRD检测试剂盒,已被纳入中国国家药品监督管理局(NMPA)创新医疗器械特别审查程序。
PART 02 卵巢癌的一线维持治疗
卵巢癌一线维持治疗,是指针对新诊断卵巢癌患者经初始化疗达到临床完全缓解(CR)或部分缓解(PR)后,所给予的后续维持性治疗手段,其核心目的在于延缓肿瘤复发,改善患者的生存预后。化疗药物用于维持治疗的临床获益尚不明确,目前已不再推荐用于临床实践。抗血管生成药物贝伐珠单抗用于维持治疗时,需在初始化疗阶段同步联合使用;除高复发风险人群外,该药物对普通患者无进展生存期(PFS)的延长效果有限,仅能实现3~4个月的获益。近年来,PARP抑制剂在卵巢癌一线维持治疗领域完成了多项Ⅲ期随机对照临床试验,证实其疗效显著,目前已成为特定卵巢癌患者群体一线维持治疗的标准方案。
2.1奥拉帕利相关研究
2.1.1SOLO-1研究
针对携带BRCA1/2基因突变的晚期上皮性卵巢癌(epithelial ovarian cancer,EOC)患者,一项Ⅲ期随机对照临床试验对比了初始治疗有效后应用奥拉帕利与安慰剂进行维持治疗的疗效。全球数据显示,中位随访时间达41个月时,与安慰剂组相比,奥拉帕利组患者的复发或死亡风险显著降低70%;两组的3年无进展生存期(PFS)率分别为60%和27% [风险比(hazard ratio,HR)=0.30,95% CI:0.23~0.41,P<0.001],患者中位复发时间被推迟至3年以上。无论手术时机、化疗反应状态及残留病灶大小如何,接受奥拉帕利维持治疗的晚期卵巢癌患者均可获得显著的PFS获益。5年随访数据进一步证实,奥拉帕利组与安慰剂组的中位PFS分别为56.0个月和13.8个月,前者复发或死亡风险降低67%(HR=0.33,95% CI:0.25~0.43);两组的5年PFS率分别为48%和21%,且这种PFS获益在高风险与低风险亚组中均保持一致。随访至7年时,奥拉帕利组患者的中位总生存期(OS)尚未达到(not reached,NR),安慰剂组则为75.2个月,奥拉帕利组复发或死亡风险降低45%(HR=0.55,95% CI:0.40~0.76,P=0.0004);两组的7年OS率分别为67%和46.5%。此外,中国人群的疗效与安全性数据(独立盲法评估的HR=0.39,95% CI:0.17~0.86,P=0.0168)与全球数据基本保持一致。
2.1.2PAOLA-1研究
本项Ⅲ期随机对照临床试验入组一线含铂化疗联合贝伐珠单抗治疗有效的晚期上皮性卵巢癌(EOC)患者,旨在探讨贝伐珠单抗单药维持治疗与贝伐珠单抗联合奥拉帕利维持治疗的疗效差异,中位随访22.9个月的数据显示,贝伐珠单抗联合奥拉帕利组与贝伐珠单抗联合安慰剂组相比,BRCA突变患者的中位PFS分别为37.2个月和21.7个月(HR=0.31,95%CI:0.20~0.47),BRCA野生型/HRD阳性患者的中位PFS分别为28.1个月和16.6个月(HR=0.43,95%CI:0.28~0.66),而BRCA野生型/HRD阴性或状态未知患者的中位PFS分别为16.9个月和16.0个月(HR=0.92,95%CI:0.72~1.17),组间差异无统计学意义;5年随访数据进一步验证,BRCA突变患者中联合奥拉帕利组与安慰剂组的中位PFS分别为60.7个月和21.7个月(HR=0.45,95%CI:0.32~0.64),5年OS率分别为73.2%和53.8%,中位OS分别为75.2个月和66.9个月(HR=0.60,95%CI:0.39~0.93),BRCA野生型/HRD阳性患者的中位PFS分别为30.0个月和16.6个月(HR=0.47,95%CI:0.32~0.70),5年OS率分别为54.7%和44.2%,中位OS分别为未达到(NR)和52个月(HR=0.71,95%CI:0.45~1.13),BRCA野生型/HRD阴性或状态未知患者的中位PFS分别为17.3个月和16.0个月(HR=0.90,95%CI:0.72~1.13),5年OS率分别为25.7%和32.3%,中位OS分别为36.8个月和40.4个月(HR=1.19,95%CI:0.88~1.63),该研究证实,在贝伐珠单抗维持治疗基础上联用奥拉帕利,可为BRCA突变及BRCA野生型/HRD阳性的晚期EOC患者带来显著获益,但对BRCA野生型/HRD阴性(双阴性)患者无额外获益,且亚组分析显示,无论手术时机或术后残留病灶状况如何,相较于贝伐珠单抗单药,联合治疗方案均可改善患者PFS,其中接受初始肿瘤细胞减灭术且术后无肉眼残留病灶的患者获益最为显著,而在HRD阳性患者群体中,无论国际妇产科联盟(FIGO)分期、疾病进展风险高低及年龄差异,贝伐珠单抗联合奥拉帕利的维持治疗方案均能显著延长患者PFS。
2.1.3一项国内多中心的真实世界研究结果
对于新诊断的BRCA野生型/HRD阳性卵巢癌患者,奥拉帕利单药维持治疗的中位无进展生存期(PFS)达21个月,1年PFS率为75.2%,这一结果表明,奥拉帕利能够为中国该类患者人群提供新的治疗选择。
2.1.4DUO-O研究
本项Ⅲ期随机安慰剂对照研究针对BRCA野生型新诊断晚期卵巢癌患者开展,设置三组治疗方案:组1为化疗联合贝伐珠单抗治疗后,予贝伐珠单抗单药维持治疗;组2为化疗联合贝伐珠单抗+度伐利尤单抗治疗后,予贝伐珠单抗+度伐利尤单抗联合维持治疗;组3为化疗联合贝伐珠单抗+度伐利尤单抗治疗后,予贝伐珠单抗+度伐利尤单抗+奥拉帕利三药联合维持治疗,随访近3年的结果显示,意向治疗(ITT)人群中,组3与组1的中位无进展生存期(PFS)分别为25.1个月和19.3个月(HR=0.61,95%CI:0.51~0.73),其中BRCA野生型HRD阳性人群的中位PFS分别为45.1个月和23.3个月(HR=0.46,95%CI:0.33~0.65),HRD阴性人群的中位PFS分别为20.9个月和17.4个月(HR=0.68,95%CI:0.54~0.86),该研究证实,与对照组相比,一线化疗联合贝伐珠单抗+度伐利尤单抗,后续序贯贝伐珠单抗+度伐利尤单抗+奥拉帕利维持治疗的方案可显著改善患者PFS。
2.2尼拉帕利相关研究
2.2.1PRIMA研究
BRCA野生型/HRD阳性患者中,两组中位无进展生存期(PFS)分别为19.6个月和8.2个月(HR=0.50,95%CI:0.31~0.83,P=0.006);BRCA野生型/HRD阴性(HRP)患者的中位PFS分别为8.1个月和5.4个月(HR=0.68,95%CI:0.49~0.94,P=0.020),其获益程度显著低于BRCA突变及HRD阳性患者,PRIMA研究显示,无论年龄分组、手术时机及术后残留病灶状况如何,接受尼拉帕利维持治疗的晚期卵巢癌患者均可获得PFS改善,6年随访数据表明:HRD阳性患者中,安慰剂组后续接受PARP抑制剂(PARPi)治疗的比例为48.4%,尼拉帕利组5年PFS率为安慰剂组的2倍(35%vs16%),两组中位总生存期(OS)分别为71.9个月和69.8个月(HR=0.95);HRP患者中,安慰剂组后续接受PARPi治疗的比例为18.8%,尼拉帕利组与安慰剂组中位OS分别为36.6个月和32.2个月(HR=0.93),该研究结果显示,意向治疗(ITT)人群中两组的OS无显著差异。
2.2.2PRIME研究
本研究是尼拉帕利在中国新诊断晚期卵巢癌患者中开展的多中心、随机、安慰剂对照Ⅲ期临床试验,与PRIMA研究相比,其独特之处在于无论患者术后残余病灶状态如何均可入组,且纳入了FIGOⅢ期初次减瘤术后无残余病灶的卵巢癌患者,同时对全人群采用尼拉帕利个体化起始剂量给药;结果显示,尼拉帕利组与安慰剂组相比,整体人群的中位无进展生存期(PFS)分别为24.8个月和8.3个月(HR=0.45,95%CI:0.34~0.60,P<0.001),胚系BRCA(gBRCA)突变患者的中位PFS分别为未达到(NR)和10.8个月(HR=0.40,95%CI:0.23~0.68,P<0.001),非gBRCA突变/HRD阳性患者的中位PFS分别为24.8个月和11.1个月(HR=0.58,95%CI:0.36~0.93,P=0.022),HRD阴性患者的中位PFS分别为16.6个月和5.5个月(HR=0.41,95%CI:0.22~0.75),且无论患者一线含铂化疗后是否达到临床完全缓解(CR)或部分缓解(PR),尼拉帕利均能较安慰剂显著延长患者PFS时间。
2.2.3一项前瞻性中国多中心真实世界研究RENI-1结果
在全患者人群中,无论BRCA突变状态或HRD状态如何,尼拉帕利一线维持治疗均能带来无进展生存期(PFS)获益;其中BRCA突变及HRD阳性患者的获益尤为显著。
2.2.4OVARIO研究
本研究为一项Ⅱ期单臂临床试验,旨在评估尼拉帕利联合贝伐珠单抗用于新诊断晚期卵巢癌患者一线维持治疗的疗效,主要研究终点设定为18个月无进展生存期(PFS)率。研究结果显示,整体人群的18个月、24个月PFS率分别为62%和53%;其中HRD阳性人群的18个月、24个月PFS率分别达76%和63%,HRD阴性人群分别为47%和42%,HRD状态未知人群则分别为56%和50%。中位随访时间28.7个月时,整体人群的中位PFS为19.6个月;进一步分层分析可见,BRCA突变人群中位PFS未达到(NR),BRCA野生型/HRD阳性人群为28.3个月,HRD阴性人群为14.2个月,HRD状态未知人群为12.1个月。该研究初步证实,尼拉帕利联合贝伐珠单抗的方案应用于新诊断晚期卵巢癌患者的一线维持治疗,能够为患者带来明确获益。
2.3氟唑帕利相关研究
FZOCUS-1研究是一项随机、双盲、安慰剂对照的Ⅲ期临床研究,旨在评估氟唑帕利单药或联合阿帕替尼用于晚期卵巢癌一线维持治疗的疗效与安全性。研究结果显示,氟唑帕利单药组与安慰剂组相比,整体人群的中位无进展生存期(PFS)分别为未达到(NR)和11.1个月(HR=0.49,95%CI:0.37~0.67,P<0.0001);胚系BRCA(gBRCA)突变患者的中位PFS分别为未达到(NR)和14.9个月(HR=0.40,95%CI:0.22~0.73,P=0.0009);非gBRCA突变患者的中位PFS分别为25.5个月和8.4个月(HR=0.53,95%CI:0.37~0.75,P=0.0001)。该研究证实,氟唑帕利单药用于晚期上皮性卵巢癌(EOC)患者的一线维持治疗,能够为全人群带来不同程度的显著获益。
2.4塞纳帕利相关研究
FLAMES研究是一项随机、双盲、安慰剂对照、多中心的Ⅲ期临床研究,结果显示:塞纳帕利组与安慰剂组相比,整体人群的中位无进展生存期(PFS)分别为未达到(NR)和13.6个月(HR=0.43,95%CI:0.32~0.58,P<0.001);BRCA突变患者的中位PFS分别为NR和15.6个月(HR=0.43,95%CI:0.24~0.76,P<0.001);BRCA野生型患者的中位PFS分别为NR和12.9个月(HR=0.43,95%CI:0.30~0.61,P<0.001)。事后分析进一步表明,BRCA野生型/HRD阳性患者的中位PFS分别为NR和12.9个月(HR=0.30,95%CI:0.15~0.60);BRCA野生型/HRD阴性患者的中位PFS分别为27.1个月和19.5个月(HR=0.74,95%CI:0.36~1.54)。该研究证实,塞纳帕利用于晚期卵巢癌一线维持治疗,可使BRCA突变及BRCA野生型/HRD阳性患者的PFS获得显著获益。
基于上述研究证据,推荐相应PARP抑制剂用于一线维持治疗(表4)。

PART 03复发性卵巢癌的维持治疗
卵巢癌复发主要分为铂敏感复发和铂耐药复发两类,前者指化疗结束后6个月及以上出现的复发,后者指化疗结束后不足6个月的复发;初始治疗后疾病未得到控制,呈持续性或进展性发展的患者,亦归为铂耐药范畴。铂敏感复发的治疗原则为继续采用以铂类为基础的联合化疗;铂耐药复发者则一般不优先推荐含铂化疗,多选用非铂类化疗药物进行治疗。复发患者经治疗达到缓解后,可考虑实施维持治疗,旨在推迟复发时间、降低复发风险。长期以来,可用于复发性卵巢癌维持治疗的药物选择较为有限,贝伐珠单抗维持治疗的疗效持续时间较短;近年来,PARP抑制剂在铂敏感复发卵巢癌维持治疗领域的研究取得重大突破,目前已被列为铂敏感复发卵巢癌维持治疗的标准方案。
3.1奥拉帕利相关研究
3.1.1Study19研究
针对铂敏感复发卵巢癌患者的一项Ⅱ期研究显示,奥拉帕利维持治疗组与安慰剂组的中位无进展生存期(PFS)分别为8.4个月和4.8个月(HR=0.35,95%CI:0.25~0.49,P<0.001)。亚组分析结果表明,BRCA突变患者的中位PFS分别为11.2个月和4.3个月(HR=0.18,95%CI:0.10~0.31,P<0.0001);BRCA野生型患者的中位PFS则分别为7.4个月和5.5个月(HR=0.54,95%CI:0.34~0.85,P=0.0075)。总生存(overall survival,OS)分析数据显示,奥拉帕利组与安慰剂组的中位OS分别为29.8个月和27.8个月[HR=0.73,95%CI:0.55~0.95,P=0.02138(未达预设统计学差异阈值)];探索性限制性分析结果则显示,两组的中位OS分别为41.6个月和35.3个月。进一步亚组OS分析可见,BRCA突变患者的中位OS分别为34.9个月和30.2个月(HR=0.62,95%CI:0.42~0.93,P=0.02140);BRCA野生型患者的中位OS分别为24.5个月和26.6个月(HR=0.84,95%CI:0.57~1.25,P=0.39749)。该研究初步证实,奥拉帕利维持治疗可为铂敏感复发卵巢癌患者带来获益。
3.1.2SOLO-2研究
本研究是一项针对胚系BRCA(gBRCA)突变铂敏感复发卵巢癌患者的Ⅲ期临床研究,结果显示,奥拉帕利组与安慰剂组的中位无进展生存期(PFS)分别为19.1个月和5.5个月(HR=0.30,95%CI:0.22~0.41,P<0.0001);经独立盲法评估的中位PFS则分别为30.2个月和5.5个月(HR=0.25,95%CI:0.18~0.35,P<0.0001)。总生存期(OS)分析数据显示,奥拉帕利组与安慰剂组的中位OS分别为51.7个月和38.8个月(HR=0.74,95%CI:0.54~1.00,P=0.054);鉴于安慰剂组中有38%的患者后续接受了PARP抑制剂治疗,校正该交叉用药因素后,两组的中位OS分别为51.7个月和35.4个月(HR=0.56,95%CI:0.35~0.97)。本研究首次证实,奥拉帕利维持治疗能够为gBRCA突变铂敏感复发卵巢癌患者带来显著的OS获益。
3.1.3OPINION研究
本研究为一项针对非胚系BRCA(gBRCA)突变铂敏感复发卵巢癌患者的Ⅲb期临床研究,主要分析结果显示,奥拉帕利维持治疗下整体人群的中位无进展生存期(PFS)达9.2个月。亚组分析进一步表明,体细胞BRCA(sBRCA)突变患者的中位PFS为16.4个月;同源重组缺陷(HRD)阳性人群(含sBRCA突变患者)的中位PFS为11.1个月;HRD阳性人群(排除sBRCA突变患者)的中位PFS为9.7个月;HRD阴性患者的中位PFS则为7.3个月。本研究进一步补充证实,奥拉帕利维持治疗对非gBRCA突变铂敏感复发卵巢癌患者同样具备确切有效性。
3.1.4L-MOCA研究
本研究为一项针对亚洲铂敏感复发卵巢癌患者的Ⅲ期单臂临床研究,其中中国患者占比达91.5%,研究结果显示,奥拉帕利维持治疗下整体人群的中位无进展生存期(PFS)为16.1个月,预估6个月和12个月PFS率分别为76.0%和57.1%;进一步亚组分析可见,BRCA突变患者中位PFS为21.2个月,胚系BRCA(gBRCA)突变患者中位PFS为21.4个月,BRCA野生型患者中位PFS为11.0个月。针对既往接受二线治疗的患者亚组分析显示,其中位PFS可达18.0个月,其中二线BRCA突变患者中位PFS为24.9个月,二线BRCA野生型患者中位PFS为14.1个月,与全人群亚组分析结果趋势一致。中期总生存期(OS)数据[47]显示,中位随访时间40个月时,意向治疗(ITT)人群中位OS达54.4个月,42个月OS率为59.7%;其中BRCA突变亚组中位OS尚未达到(51.9个月-NE),BRCA野生型/HRD阳性亚组与HRD阴性(HRP)亚组的中位OS分别为54.6个月和37.2个月。该研究证实,无论BRCA突变状态如何,奥拉帕利维持治疗均可使亚洲铂敏感复发卵巢癌患者显著获益。
值得注意的是,美国FDA基于其他PARP抑制剂用于非BRCA突变患者铂敏感复发维持治疗后存在潜在死亡风险增加的相关数据,将奥拉帕利的适应证同样限制于BRCA突变人群;而目前中国地区奥拉帕利针对铂敏感复发卵巢癌人群的适应证尚未发生调整。
3.2尼拉帕利相关研究
3.2.1NOVA研究
本研究针对铂敏感复发卵巢癌患者开展,所有入组患者均采用尼拉帕利300mg/d固定起始剂量治疗,结果显示,尼拉帕利组与安慰剂组相比,胚系BRCA(gBRCA)突变患者的中位无进展生存期(PFS)分别为21.0个月和5.5个月(HR=0.27,95%CI:0.17~0.41,P<0.001);gBRCA野生型/HRD阳性患者的中位PFS分别为12.9个月和3.8个月(HR=0.38,95%CI:0.24~0.59,P<0.001);BRCA野生型/HRD阳性患者的中位PFS分别为9.3个月和3.7个月(HR=0.38,95%CI:0.23~0.63,P<0.001);BRCA野生型/HRD阴性患者的中位PFS分别为6.9个月和3.8个月(HR=0.58,95%CI:0.36~0.92,P=0.02)。该研究证实,尼拉帕利维持治疗能够为不同BRCA及HRD状态的铂敏感复发卵巢癌患者带来程度不一的生存获益。在NOVA研究中,无论患者年龄分组、化疗反应状态如何,无论是gBRCA突变还是非gBRCA突变人群,接受尼拉帕利维持治疗的铂敏感复发患者均可获得PFS改善。总生存期(OS)分析数据显示,尼拉帕利组与安慰剂组相比,gBRCA突变患者的中位OS分别为40.9个月和48.1个月(HR=0.85,95%CI:0.61~1.20),且安慰剂组中有39.2%的患者后续接受了PARP抑制剂治疗;非gBRCA突变患者的中位OS则分别为31.0个月和34.8个月(HR=1.06,95%CI:0.81~1.37)。基于NOVA研究中非gBRCA突变患者队列OS次要终点的风险比为1.06(95% CI:0.81~1.37),目前美国FDA已将尼拉帕利用于铂敏感复发卵巢癌维持治疗的适应证,限制于gBRCA突变人群。
3.2.2NORA研究
本研究为一项针对中国铂敏感复发卵巢癌患者、采用尼拉帕利个体化起始剂量的Ⅲ期随机对照研究。结果显示,整体人群中尼拉帕利组与安慰剂组的中位无进展生存期(PFS)分别为18.3个月和5.4个月(HR=0.32,95%CI:0.23~0.45,P<0.0001)。亚组分析表明,尼拉帕利组与安慰剂组相比,胚系BRCA(gBRCA)突变患者的中位PFS分别为未达到(NR)和5.5个月(HR=0.22,95%CI:0.12~0.39,P<0.0001);非gBRCA突变患者的中位PFS分别为11.1个月和3.9个月(HR=0.40,95%CI:0.26~0.61,P<0.0001)。该研究证实,采用尼拉帕利个体化起始剂量能够为不同BRCA状态的中国铂敏感复发卵巢癌患者带来生存获益。在NORA研究中,无论患者化疗反应状态、前次含铂化疗后6~12个月或≥12个月疾病进展,无论是gBRCA突变还是非gBRCA突变人群,接受尼拉帕利维持治疗的铂敏感复发患者均可获得PFS改善;此外,无论患者是否接受二次肿瘤细胞减灭术,尼拉帕利维持治疗均能显著改善其PFS。总生存期(OS)最终分析数据显示,整体人群中尼拉帕利组与安慰剂组的中位OS分别为51.5个月和47.6个月(HR=0.86,95%CI:0.60~1.23),且安慰剂组中有46.6%的患者后续接受了PARP抑制剂治疗;gBRCA突变患者的中位OS分别为56.0个月和47.6个月(HR=0.86,95%CI:0.46~1.58),安慰剂组中该比例达57.1%;非gBRCA突变患者的中位OS分别为46.5个月和46.9个月(HR=0.87,95%CI:0.56~1.35),安慰剂组后续接受PARP抑制剂治疗的比例为39.6%。采用符合方案分析(Per-protocol Analysis,PP分析)时,非gBRCA突变患者的中位OS分别为50.6个月和46.9个月(HR=0.84,95%CI:0.54~1.32)。该研究提示,尼拉帕利个体化起始剂量有望为不同BRCA状态的中国铂敏感复发卵巢癌患者带来OS获益趋势,目前中国获批的尼拉帕利用于铂敏感复发卵巢癌人群的适应证尚未发生调整。
3.3氟唑帕利相关研究FOZCUS-2研究
本研究为一项针对铂敏感复发卵巢癌患者维持治疗的Ⅲ期临床研究,其更新结果显示,氟唑帕利组与安慰剂组的中位无进展生存期(PFS)分别为15.7个月和5.5个月(HR=0.31,95%CI:0.22~0.44,P<0.0001);亚组分析表明,氟唑帕利组与安慰剂组相比,胚系BRCA(gBRCA)突变人群的中位PFS分别为18.4个月和5.2个月(HR=0.18,95%CI:0.10~0.31,P<0.0001),非gBRCA突变人群的中位PFS分别为13.6个月和5.5个月(HR=0.57,95%CI:0.38~0.86)。该研究证实,氟唑帕利维持治疗能够为不同BRCA状态的中国铂敏感复发卵巢癌患者带来显著的PFS获益。
3.4PARP抑制剂维持治疗后的再次维持治疗
OReO研究是一项Ⅲb期随机对照研究,针对既往接受过多线治疗、曾行一次PARP抑制剂维持治疗,且末次含铂化疗达到临床完全缓解(CR)/部分缓解(PR)的复发性卵巢癌患者,探讨再次应用奥拉帕利维持治疗的疗效。结果显示,奥拉帕利再次维持治疗组与安慰剂组相比,BRCA突变患者的中位无进展生存期(PFS)分别为4.3个月和2.8个月(HR=0.57,95%CI:0.37~0.87,P=0.022);非BRCA突变患者的中位PFS分别为5.3个月和2.8个月(HR=0.43,95%CI:0.26~0.71,P=0.0023),其中BRCA野生型/HRD阳性患者的中位PFS分别为5.3个月和2.8个月(HR=0.52,95%CI:0.26~1.10),BRCA野生型/HRD阴性患者的中位PFS分别为5.4个月和2.8个月(HR=0.49,95%CI:0.21~1.23)。该研究表明,奥拉帕利再次维持治疗可为不同BRCA及HRD状态的患者带来不同程度的PFS获益;值得注意的是,非BRCA突变组的PFS获益略优于BRCA突变组,经分析,这可能与非BRCA突变组中不同种类PARP抑制剂先后使用的比例高于BRCA突变组有关。
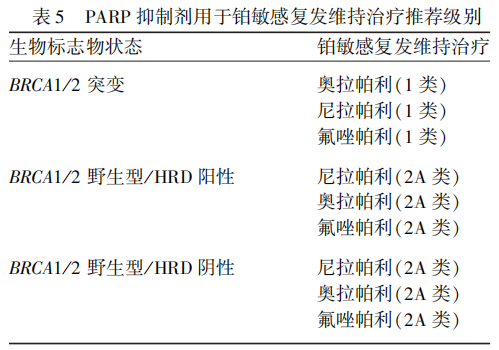
基于上述临床研究证据,本指南推荐相应PARP抑制剂用于铂敏感复发卵巢癌的维持治疗(见表5);对于铂敏感复发的BRCA突变患者,若既往接受PARP抑制剂维持治疗后未进展,推荐可再次应用PARP抑制剂维持治疗(2A类推荐)。
PART 04复发性卵巢癌的后线治疗
既往接受过二线及以上化疗的复发性卵巢癌患者,其后续治疗被定义为后线治疗。此类患者普遍一般状况欠佳,对治疗药物的敏感性较低,且临床可选择的有效治疗药物相对匮乏。相较于细胞毒性化疗药物,PARP抑制剂的毒性更低,用于后线治疗具备独特优势。目前多种PARP抑制剂已相继获得美国FDA或中国NMPA批准,用于多次复发卵巢癌的后线治疗,为该类患者提供了“去化疗”的治疗方案。
4.1铂敏感复发卵巢癌的治疗
对铂敏感复发卵巢癌患者应该首选含铂化疗方案,但对于难以耐受含铂化疗、对铂类药物过敏、不再同意接受化疗者,有必要探索其他替代治疗方案。
4.1.1奥拉帕利相关研究
4.1.1.1 SOLO-3研究
该研究是应用奥拉帕利单药治疗既往接受了二线及以上化疗的gBRCA突变铂敏感复发卵巢癌患者的Ⅲ期随机对照研究,结果显示,与由医生自主决定的不含铂类的化疗方案相比,奥拉帕利单药治疗显著提高了患者的客观缓解率(objective response rate,ORR)[72.2%vs51.4%,比值比(odds ratio,OR)=2.53,95%CI:1.40~4.58,P=0.002],奥拉帕利组和化疗组的独立盲法评估的中位PFS时间分别为13.4个月和9.2个月(HR=0.62,95%CI:0.43~0.91,P=0.013)。最终生存分析显示,奥拉帕利组和化疗组患者的中位OS时间分别为34.9个月和32.9个月,两组比较差异无统计学意义(HR=1.07,95%CI:0.76~1.49,P=0.714),可能与25%的化疗组患者提前退出研究影响评估OS相关。但SOLO-3研究中≥3线化疗亚组分析提示,奥拉帕利组和化疗组的OS分别为29.9个月和39.4个月(HR=1.33,95%CI:0.84~2.18)。
4.1.1.2 CLIO研究
在BRCA野生型铂敏感复发的EOC患者中,与标准治疗(卡铂联合多柔比星脂质体/吉西他滨)相比,奥拉帕利单药治疗的ORR、疾病控制率、中位PFS时间、中位OS时间比较差异均无统计学意义。
4.1.1.3 LIGHT研究
是基于BRCA突变和HRD状态评估铂敏感复发EOC患者接受奥拉帕利治疗的研究。结果显示,gBRCA突变、sBRCA突变、BRCA野生型/HRD阳性、BRCA野生型/HRD阴性患者的ORR分别为69%、64%、29%、10%;中位PFS时间分别为11.0个月、10.8个月、7.2个月、5.4个月;18个月的OS率分别为88.0%、86.4%、78.6%、59.6%。
4.1.2尼拉帕利相关研究
4.1.2.1 QUADRA研究
在尼拉帕利单药治疗既往接受过三线及以上治疗的铂敏感复发卵巢癌患者中,BRCA突变患者的ORR为39%,HRD阳性患者的ORR为26%。
4.1.2.2 AVANOVA2研究
该研究是一项比较尼拉帕利联合贝伐珠单抗或尼拉帕利单药治疗不限既往治疗线数的铂敏感复发EOC患者的Ⅱ期随机对照研究。结果显示,中位随访时间16.9个月,在尼拉帕利联合贝伐珠单抗治疗组和尼拉帕利单药治疗组中,患者的中位PFS时间分别为11.9个月和5.5个月(HR=0.35,95%CI:0.21~0.57,P<0.0001),ORR分别为60%和27%(OR=4.23,P=0.001)。其中,BRCA突变患者中位PFS时间分别为14.4个月和9.0个月(HR=0.49,95%CI:0.21~1.15);BRCA野生型/HRD阳性患者中位PFS时间分别为11.9个月和4.1个月(HR=0.19,95%CI:0.06~0.59);BRCA野生型/HRD阴性患者中位PFS时间分别为11.3个月和4.2个月(HR=0.40,95%CI:0.19~0.85)。生存分析显示,尼拉帕利联合贝伐珠单抗治疗组和尼拉帕利单药治疗组患者的中位OS时间分别为29.4个月和27.8个月(HR=0.75,95%CI:0.44~1.28,P=0.30)。
4.1.3氟唑帕利相关研究
FZOCUS-3研究应用氟唑帕利治疗既往2~4线含铂化疗的gBRCA突变铂敏感复发EOC患者,结果显示:独立评审委员会(Independent Review Committee,IRC)和研究者评估的ORR分别为69.9%和70.8%;中位PFS时间分别为12.0个月和10.3个月。中位OS时间尚未达到,12个月和18个月OS率分别为93.7%和89.2%。
4.1.4帕米帕利相关研究
在BGB-290-102研究中,应用帕米帕利治疗既往二线及以上含铂化疗的gBRCA突变的铂敏感复发EOC患者,结果显示:IRC和研究者评估的ORR分别为64.6%和62.2%;IRC评估的中位PFS时间为15.2个月。中位OS时间尚未达到,6个月和12个月OS率分别为93.2%和83.5%。
4.1.5塞纳帕利相关研究
SABRINA研究探索塞纳帕利治疗既往二线及以上含铂化疗的BRCA突变的铂敏感复发EOC患者,结果显示:IRC和研究者评估的ORR分别为66.3%和58.7%;IRC评估的中位PFS为11.1个月;中位OS时间尚未达到。
4.2铂耐药复发卵巢癌的治疗
铂耐药复发卵巢癌患者对含铂化疗方案一般不再敏感,原则上推荐非铂化疗,但临床反应率十分有限,多在20%左右。一旦铂耐药复发,患者往往难以治愈,在姑息治疗的同时必须兼顾生活质量,比化疗药物毒性较低的PARP抑制剂对于BRCA突变患者是一种“去化疗”的治疗选择。
4.2.1奥拉帕利相关研究
4.2.1.1 Study42研究
对既往接受三线及以上含铂化疗方案的BRCA突变铂耐药复发卵巢癌患者给予奥拉帕利治疗,ORR达31.1%。奥拉帕利是第一个在复发性卵巢癌治疗中表现出临床疗效的PARP抑制剂。
4.2.1.2 CLIO研究
针对铂耐药复发卵巢癌患者,奥拉帕利单药治疗组患者的ORR高于化疗组(18%vs6%),但尚未有统计学意义;亚组分析提示BRCA突变型患者较野生型患者获益显著。
4.2.2尼拉帕利相关研究
4.2.2.1 QUADRA研究
尼拉帕利单药治疗铂耐药复发卵巢癌,BRCA突变患者、HRD阳性患者和HRD阴性/未知患者的ORR分别为27%、10%和3%,这提示尼拉帕利对BRCA突变铂耐药复发卵巢癌有一定疗效。
4.2.2.2 TOPACIO研究
尼拉帕利联合帕博利珠单抗治疗铂耐药复发/难治性卵巢癌患者的ORR为18%,疾病控制率为65%,治疗效果不受BRCA状态的影响。
4.2.2.3 ANNIE研究
尼拉帕利联合安罗替尼治疗铂耐药复发性卵巢癌疗效可评估者的ORR为50.0%,中位PFS时间为9.2个月,OS最终分析中位时间为18.2个月。该研究初步表明此种联合治疗可作为耐药复发卵巢癌的一种新选择。
4.2.3帕米帕利相关研究
在BGB-290-102研究中,帕米帕利用于治疗既往接受过二线及以上含铂化疗的胚系BRCA(gBRCA)突变铂耐药复发上皮性卵巢癌(EOC)患者,结果显示:独立评审委员会(IRC)和研究者评估的客观缓解率(ORR)分别为31.6%和26.3%;IRC评估的中位无进展生存期(PFS)为6.2个月,中位总生存期(OS)为13.6个月,6个月和12个月OS率分别为73.4%和50.5%。基于该研究数据,帕米帕利在国内率先获批铂耐药复发卵巢癌后线治疗适应证。
由于SOLO-3研究中奥拉帕利组未显示OS获益,美国FDA已撤回其卵巢癌后线治疗适应证;尼拉帕利后线治疗相关的QUADRA研究为单臂设计,缺乏对照数据支持OS获益,其后线治疗适应证也被美国FDA撤回。中国NMPA从未批准过奥拉帕利、尼拉帕利的卵巢癌后线治疗适应证,目前国内仅有氟唑帕利、帕米帕利两款PARP抑制剂获批用于复发性卵巢癌的后线治疗。
基于上述研究证据,本指南推荐相应PARP抑制剂用于复发性卵巢癌的后线治疗(见表6)。

PART 05 PARP抑制剂在新辅助治疗中的探索研究
NANT研究是尼拉帕利单药用于HRD阳性晚期卵巢癌新辅助治疗的Ⅱ期单臂、多中心研究。研究共入组67例患者,48例完成新辅助治疗及疗效评估,客观缓解率(ORR)为62.5%,疾病控制率(DCR)为87.5%;其中BRCA突变患者亚组(n=22)的ORR和DCR分别达77.3%和100.0%。40例患者完成中间型肿瘤细胞减灭术(IDS),80.0%实现R0切除;BRCA突变患者亚组(n=21)的R0切除率为85.7%。
NOW研究旨在明确奥拉帕利单药用于胚系BRCA1/2、RAD51C/D、PALB2突变卵巢癌新辅助治疗的可行性。研究入组15例患者,13例可进行疗效评估,部分缓解(PR)率为53.8%,12个月无进展生存期(PFS)率为81.0%;14例患者接受IDS治疗,85.7%实现R0切除。
NEO研究是奥拉帕利用于铂敏感复发性高级别浆液性卵巢癌新辅助治疗的Ⅱ期随机、多中心临床研究。术前经短疗程奥拉帕利治疗后,共41例患者行再次肿瘤细胞减灭术,随后随机分为奥拉帕利治疗组和化疗后序贯奥拉帕利维持治疗组。研究提示,对于病灶完全切除的患者,单独使用奥拉帕利与化疗后序贯奥拉帕利的疗效相当,且毒性更低。
一项研究探索了奥拉帕利联合帕博利珠单抗用于HRD阳性新诊断晚期卵巢癌的新辅助治疗,共入组20例患者,整体ORR为70%,其中BRCA突变患者的ORR达84.6%。
一项帕米帕利联合索凡替尼用于新诊断晚期卵巢癌新辅助治疗的Ⅱ期研究显示,该联合方案的ORR为100%(均为PR),R0切除率达90%(18/20),其余2例为R1切除。在18例R0切除患者中,11例为BRCA突变,6例为BRCA野生型/HRD阳性,1例为HRD阴性;其中1例BRCA突变患者达到病理完全缓解。
上述研究均为小样本非随机对照研究,初步提示PARP抑制剂单药或联合治疗有望替代传统新辅助化疗,但该治疗模式的探索仍需进一步证实患者的总生存期(OS)实际获益。目前现有证据尚不足以推荐PARP抑制剂单药或联合治疗用于新诊断、铂敏感复发卵巢癌患者的新辅助治疗。PARP抑制剂用于一线、二线维持治疗及后线治疗的具体药物用法见表7。

PART 06PARP 抑制剂使用的安全性管理
6.1PARP抑制剂的常见不良反应及其处理
在PARP抑制剂用药过程中,大部分患者会出现不同程度的不良反应,特点如下:
(1)不良反应以轻度或中度为主,即不良事件通用术语标准(common terminology criteria for adverse events,CTCAE)毒性分级1~2级更为常见,患者耐受性高于化疗(细胞毒性药物)。
(2)大部分不良反应出现在服药前期(前3个月),随着用药时间逐渐延长,患者耐受,不良反应的程度逐渐减弱。
(3)PARP抑制剂的不良反应呈现剂量相关性,大部分不良反应通过减量、对症治疗等方法可控制。
(4)血液学、胃肠道不良反应及疲劳最常见。大部分3~4级不良反应为血液学不良反应,且是调整药物剂量、中断和停止用药的最主要原因,0.9%~27.6%的患者因不良反应而终止用药,大部分患者可长期用药维持治疗。
(5)不同PARP抑制剂的药物结构、药代动力学以及代谢途径不完全一致,需要患者关注不同药物毒性特点,更好地进行预防监测和处理。
(6)奥拉帕利联合贝伐珠单抗维持治疗毒性与两种药物单独使用毒性并未出现明显的叠加效应,毒性可耐受。奥拉帕利或尼拉帕利联合贝伐珠单抗常见的不良反应为疲劳、恶心、贫血、血小板减少和高血压。3级以上不良反应发生率为48.5%~77.1%,主要为贫血、血小板减少和高血压。需要注意尼拉帕利、PARP抑制剂联合贝伐珠单抗使用相关高血压的监测和管理。
临床医生需要重视PARP抑制剂使用过程中的毒性管理,通过告知使患者对毒性有适当预知,合理地监测和处理,提高患者依从性,并减少用药中断造成的血药浓度波动,提高患者生存质量和疗效。
6.1.1血液学不良反应
使用PARP抑制剂的患者需要定期检查血常规,尤其是刚开始用药时。奥拉帕利在治疗的最初12个月内,推荐在基线以及随后的每月进行一次全血细胞计数检测。尼拉帕利建议在开始用药的第1个月内每周检测一次全血细胞计数,在接下来11个月的治疗中每月监测一次。氟唑帕利建议在治疗的最初3个月内,推荐在基线进行全血细胞计数检测以及随后每2周监测一次。帕米帕利建议在治疗的最初3个月内,每周监测一次。塞纳帕利建议在治疗的最初3个月内,推荐在基线进行全血细胞计数检测以及随后每2周监测一次。随后,定期监测治疗期间出现的具有临床意义的参数变化。根据这些变化可能需要暂停用药或减量和(或)进一步治疗。
6.1.1.1贫血
贫血是使用PARP抑制剂最常见的血液学不良反应,总体发生率为21.0%~89.4%,3~4级不良反应发生率为5.0%~41.6%。一般处理原则:
(1)血红蛋白水平降至80~100g/L者,可在监测血常规的情况下继续使用PARP抑制剂,对缺铁、叶酸缺乏患者可补充铁剂和叶酸补充剂,促红细胞生成素需谨慎使用。
(2)血红蛋白水平<80g/L者,暂停使用PARP抑制剂,对于出现贫血症状的患者必要时采用红细胞输注治疗,待血红蛋白水平恢复至≥90g/L后,下调一个剂量水平恢复PARP抑制剂使用(常用PARP抑制剂的减量方法见表8,氟唑帕利待血红蛋白恢复至≥80g/L后恢复用药,塞纳帕利待血红蛋白恢复至≥100g/L后恢复用药),恢复用药后每周监测血红蛋白水平至平稳。

(3)如果停药28d内血红蛋白仍未能恢复至可用药水平,或减量至最低剂量仍再次发生血红蛋白降至80g/L以下,应停止用药。使用帕米帕利的患者首次发生血红蛋白水平低于90g/L时,需要暂停用药,治疗直至血红蛋白水平恢复至≥90g/L,下调一个剂量水平给药。再次发生,适当的支持性治疗或暂停用药后治疗直至血红蛋白水平恢复至≥90g/L后继续40mg每日2次剂量水平用药或暂停用药后降至20mg每日2次剂量水平恢复用药;若贫血危及生命,需紧急治疗:暂停给药并遵医嘱治疗直至血红蛋白水平恢复至≥90g/L,下调一个剂量水平以20mg每日2次给药;在20mg每日2次剂量水平再次出现贫血危及生命,且贫血不是由于其他干扰事件(如胃肠道出血)引起,应停用帕米帕利。
6.1.1.2血小板减少
血小板减少的发生率为14%~70%,3~4级血小板减少的发生率为1%~34%。处理方法:
(1)血小板计数降至(50~100)×10⁹/L患者,可在监测血常规的情况下继续使用PARP抑制剂。
(2)血小板计数<50×10⁹/L者,暂停使用PARP抑制剂,待血小板计数恢复至75×10⁹/L以上(氟唑帕利待血小板计数恢复至50×10⁹/L以上),下调一个剂量水平并恢复PARP抑制剂使用。
(3)治疗可使用血小板生成素、白介素-11、血小板生成素受体激动剂等药物。血小板计数低于20×10⁹/L,有出血倾向患者予输注血小板。
(4)如果停药28d内血小板计数仍未能恢复至可用药水平,或减至用药最低剂量仍再次发生血小板减少,停止用药。
❖使用尼拉帕利患者:对体重<77kg或血小板计数<150×10⁹/L的患者,建议尼拉帕利的初始剂量为200mg/d,监测血小板计数如低于100×10⁹/L者,则暂停使用PARP抑制剂,待血小板计数恢复至100×10⁹/L以上,根据血小板计数的最低值决定恢复使用PARP抑制剂的剂量:如血小板计数最低值为(75~100)×10⁹/L,可原剂量恢复PARP抑制剂使用;如血小板计数最低<75×10⁹/L,或2次以上发生血小板计数<100×10⁹/L,减量恢复PARP抑制剂使用,每周监测血小板计数至平稳。
❖使用塞纳帕利患者:血小板计数<75×10⁹/L者,暂停使用,待血小板计数恢复至75×10⁹/L以上恢复用药或降低一个剂量水平。
6.1.1.3中性粒细胞减少
中性粒细胞减少是第3种常见的血液学不良反应,总发生率5.0%~61.1%,其中4.0%~33.6%为3~4级不良反应。处理方法:
(1)中性粒细胞计数降至(1.0~2.0)×10⁹/L,在监测血常规的情况下可继续使用PARP抑制剂。
(2)中性粒细胞计数<1.0×10⁹/L,暂停使用PARP抑制剂,必要时使用粒细胞刺激因子等药物治疗。待中性粒细胞计数恢复至1.5×10⁹/L以上,下调剂量恢复用药。使用氟唑帕利者待中性粒细胞计数恢复至1.0×10⁹/L以上,首次发生中性粒细胞缺乏且不伴发热可考虑原剂量恢复用药,2次以上发生中性粒细胞缺乏或伴发热,或伴血小板降低至75×10⁹/L以下患者需下调一个剂量水平恢复使用,恢复用药后每周监测中性粒细胞计数至平稳。
(3)中性粒细胞减少治疗可考虑使用短效重组人粒细胞集落刺激因子,如果停药28d内中性粒细胞计数仍未恢复至可用药水平,或减至用药最低剂量仍再次发生中性粒细胞计数降低至1.0×10⁹/L以下,应停止用药。
6.1.2非血液学不良反应
6.1.2.1胃肠道不良反应
恶心是最常见的胃肠道不良反应,发生率为48.0%~73.6%。其他常见胃肠道不良反应包括便秘、呕吐和腹泻,1~2级不良反应多见。预防和管理:
(1)告知患者发生恶心等胃肠道症状的可能性较大,给患者合理的预期;
(2)对症治疗,可以参照细胞毒性药物化疗引起胃肠道不良反应的管理,可使用胃肠动力药、5-羟色胺受体拮抗剂等止吐药物,必要时在睡前30~60min服用止吐药物,注意服用奥拉帕利、氟唑帕利等时应避免使用阿瑞匹坦等神经激肽-1(neurokinin-1,NK-1)抑制剂(CYP3A4中度抑制剂),PARP抑制剂在睡前服用有助于减少恶心的发生;
(3)暂停PARP抑制剂用药及减量:CTCAE2级以上不良反应经治疗后未能缓解,或出现3级以上不良反应,需暂停PARP抑制剂用药,直至不良反应降至1级或缓解,恢复PARP抑制剂用药时要考虑减量(特别是第2次暂停用药后)。PARP抑制剂剂量已减至最低、不良反应症状仍持续的患者要停止用药。
6.1.2.2疲劳
疲劳是常见的不良反应,29.2%~66.0%使用PARP抑制剂的患者有疲劳症状,大部分为1~2级症状,疲劳的持续时间可能超过最初的3个月,3级以上的疲劳症状发生率小于10%。预防和管理:
(1)给患者合理的预期,告知可能发生的疲劳症状;
(2)对症治疗,必要的镇痛、抗抑郁治疗;
(3)非药物干预,认知行为疗法和营养咨询;
(4)如果疲劳仍然持续,出现CTCAE2级以上不良反应,且处理后无法缓解,或出现3级以上不良反应,应暂停用药。待症状改善后原剂量或减量(特别是第2次暂停用药后)继续用药。对于剂量已减至最低、疲劳症状仍难以控制的患者要考虑停止用药。
6.1.2.3高血压
PARP抑制剂尤其是联合贝伐珠单抗使用过程中,部分患者会出现高血压。奥拉帕利、尼拉帕利联合贝伐珠单抗在卵巢癌一线维持治疗中,46%~50%患者出现不同程度高血压,其中17%~27%为3~4级,治疗过程中需要注意高血压监测和治疗。
尼拉帕利在卵巢癌二线维持治疗中,19.3%、8.2%的患者分别出现任意级别、3~4级高血压,大部分患者可以用降压药控制,不到1%患者因高血压停药;在中国人群,该数据分别为11.1%和1.1%。使用尼拉帕利时对高血压监测和管理:
(1)使用尼拉帕利前既往高血压得到较好控制;
(2)用药期间应监测血压和心率,前两个月内至少每周监测一次,之后每月监测一次。然后第一年内每月一次,此后定期监测;
(3)必要时采用降压药物控制血压;
(4)调整尼拉帕利用量:出现3级及以上高血压应暂停用药,28d内可控制患者,下调一个剂量水平并恢复用药;对于剂量已减至最低仍出现3级及以上高血压,超过28d无法控制患者,停止用药。
6.1.2.4 其他不良反应
几种PARP抑制剂均有头痛(5.3%~30.0%)和失眠(5.6%~31.4%)的报道,多为1~2级不良反应。较少出现的不良反应包括呼吸困难、鼻咽炎、咳嗽、心动过速和心悸;以及偶有患者出现血清肌酐水平升高和肝功转氨酶升高。其他报道的不良反应包括关节痛和背痛。对于非血液学毒性处理原则如下:1~2级不良反应,可在对症治疗、监护情况下继续使用PARP抑制剂;对3级及以上不良反应,需要暂停用药,处理待不良反应降至1级以下再恢复用药,并考虑减量,如已减至最低剂量,症状仍持续超过28d考虑终止用药。
6.1.3继发恶性肿瘤
PARP抑制剂相关临床研究显示,少数用药患者可能发生继发性恶性肿瘤,主要为骨髓增生异常综合征或急性髓系白血病,其发生率为0~8%,安慰剂组则为0~4%。这类不良事件通常发生于长期治疗后,且属于严重不良事件范畴。需注意的是,所有发生上述病变的患者,均曾接受过铂类等DNA损伤类药物治疗,部分患者还合并骨髓发育不良或其他原发性恶性肿瘤病史,因此该类继发性恶性肿瘤难以完全归因于PARP抑制剂的使用。若患者在用药期间出现难以纠正的全血细胞减少、双系细胞减少或血小板减少,且排除营养缺乏、病毒感染等其他诱因,应及时转诊至血液科完善骨髓穿刺检查;一旦确诊为骨髓增生异常综合征或急性髓系白血病,需立即停用PARP抑制剂。
6.2 PARP抑制剂与其他药物的相互作用
不同PARP抑制剂的代谢途径存在明显差异,尼拉帕利主要经羧酸酯酶代谢,奥拉帕利、氟唑帕利、帕米帕利及塞纳帕利则主要通过细胞色素P450酶途径代谢,其中奥拉帕利、氟唑帕利、塞纳帕利依赖CYP3A酶代谢,帕米帕利的代谢则主要由CYP2C8酶与CYP3A酶共同介导,基于此,临床联用药物时需遵循相应原则:服用奥拉帕利、氟唑帕利或塞纳帕利期间,不推荐联合使用伊曲康唑、克拉霉素等强效CYP3A抑制剂,针对奥瑞匹坦、环丙沙星等中效CYP3A抑制剂,服用奥拉帕利、氟唑帕利时不推荐联用,服用塞纳帕利时需慎用,若确需联用则需对PARP抑制剂进行减量调整;同时,苯妥英、利福平等强效CYP3A诱导剂可能降低奥拉帕利等药物的血药浓度,应避免联用,且治疗期间需告知患者避免食用西柚、西柚汁等含有CYP3A抑制剂的食物;此外,帕米帕利与CYP3A抑制剂联用时无需调整剂量,但因其与CYP2C8抑制剂或诱导剂联用的相关数据尚不充分,临床需谨慎使用,而尼拉帕利因主要经羧酸酯酶代谢,该酶并非临床常用药物的主要作用靶点,与其他药物的相互作用风险相对较低,不过相关安全性数据仍有待进一步补充。
PART 07 结语
PARP抑制剂是一类基于同源重组缺陷(HRD)机制、通过“合成致死”效应发挥抗肿瘤作用的靶向药物,其问世彻底改变了卵巢癌的治疗格局,推动维持治疗成为卵巢癌全程管理中的核心环节,具有里程碑式的重要意义。多项高级别随机对照临床研究证实,新诊断的晚期高级别浆液性及子宫内膜样卵巢癌患者,在初始化疗达到完全缓解(CR)或部分缓解(PR)后,接受PARP抑制剂一线维持治疗可显著获益;尤其对于BRCA基因突变或(和)HRD阳性的患者,疗效更为突出,不仅能显著延长无进展生存期(PFS),部分患者还可获得总生存期(OS)的获益。铂敏感复发卵巢癌患者在化疗达到CR或PR后,应用PARP抑制剂维持治疗同样能从中获益,不过该治疗方案目前仍以BRCA突变患者为主要适用人群。PARP抑制剂暂不常规推荐用于复发性卵巢癌的后线治疗;仅作为“去化疗”治疗策略的选择,慎重用于经严格筛选的BRCA突变或(和)HRD阳性患者。在PARP抑制剂新辅助治疗领域,目前仍处于临床研究探索阶段,暂未纳入常规临床应用范畴。PARP抑制剂的总体药物毒性显著低于细胞毒性化疗药物,但临床应用中需严格管控其血液学及非血液学毒性。除及时干预贫血、血小板减少、疲劳等常见不良反应外,对于少见的骨髓增生异常综合征、急性髓系白血病等严重不良反应,更应提高警惕、密切监测。临床实践中需严格把控PARP抑制剂的用药适应证,建议用药前常规开展BRCA基因突变检测,有条件的单位可进一步完善HRD检测,以精准指导临床用药决策、评估患者预后。临床医师需充分掌握PARP抑制剂的药代动力学特征、配伍禁忌、毒副作用及耐药机制等关键要点,重视患者用药依从性管理,从而加强卵巢癌的长期规范化治疗。
图文来源:现代妇产科进展2025年2月第34卷第2期 Prog Obstet Gynecol, Feb. 2025, Vol. 34, No. 2
责编:霍盼