上海交通大学医学院附属仁济医院狄文教授、杨帆研究员、庄光磊研究员等学者联合在《Nature Biomedical Engineering》(IF=26.6)发表重磅研究成果。团队自主研发新型三特异性抗体B7H3xCD3xPDL1,创新性地将"靶向肿瘤、激活T细胞、重塑免疫微环境" 三大功能融为一体,通过独特的IFNγ-IL-15正反馈环路,成功激活肿瘤微环境中的"旁观者T细胞",并逆转免疫抑制状态,为卵巢癌、结直肠癌等难治性实体瘤提供了全新治疗路径,相关成果获国际学界高度认可。

图源:《Nature Biomedical Engineering》
一、实体瘤免疫治疗的双重瓶颈待突破
免疫检查点抑制剂(ICIs)的问世革新了癌症治疗,但仍有大量患者对治疗无响应,核心症结在于两类难题:
1.肿瘤特异性T细胞匮乏:多数实体瘤(如胰腺癌、卵巢癌、胶质母细胞瘤)突变负荷低、新抗原不足,导致能识别肿瘤的特异性T细胞数量稀少,ICIs难以发挥作用;
2.免疫微环境抑制严重:肿瘤相关巨噬细胞等髓系细胞高表达PDL1等免疫检查点分子,释放抑制性因子,即便肿瘤中存在大量"旁观者T细胞"(非肿瘤特异性 T 细胞),其杀伤功能也被严重禁锢。
此前获批的双特异性T细胞衔接器(Bi-TCE)虽能激活旁观者T细胞,但无法破解免疫抑制微环境,在实体瘤中的疗效受限。狄文教授团队针对这一痛点,提出"激活T细胞+重塑微环境" 的双效治疗思路,研发出兼具三重靶向功能的新型抗体。
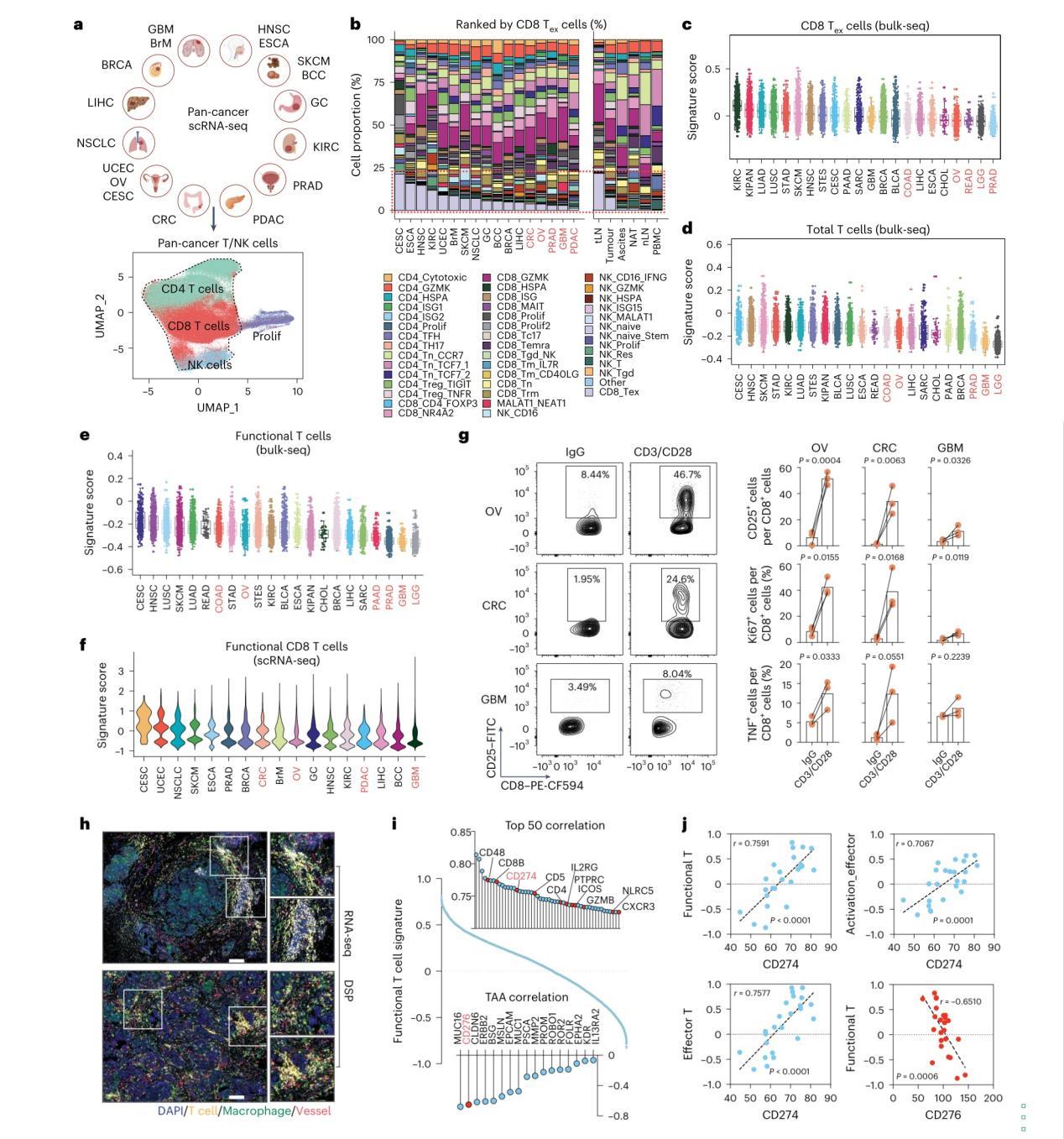
图1:免疫惰性肿瘤微环境中潜在功能性T细胞的存在
二、三特异性抗体的设计与双重作用机制
团队基于自主搭建的TROY-Ig抗体平台,成功构建B7H3xCD3xPDL1三特异性抗体,其结构设计精准适配治疗需求:
✿双Fab臂靶向泛癌抗原B7H3:确保肿瘤特异性结合,避免脱靶效应;
✿低亲和力CD3结合域:温和激活T细胞(包括旁观者T细胞),减少系统性免疫激活风险;
✿PDL1结合域:既是免疫检查点阻断剂,又是免疫细胞间的"桥梁分子",介导T细胞与髓系细胞的功能性互作。
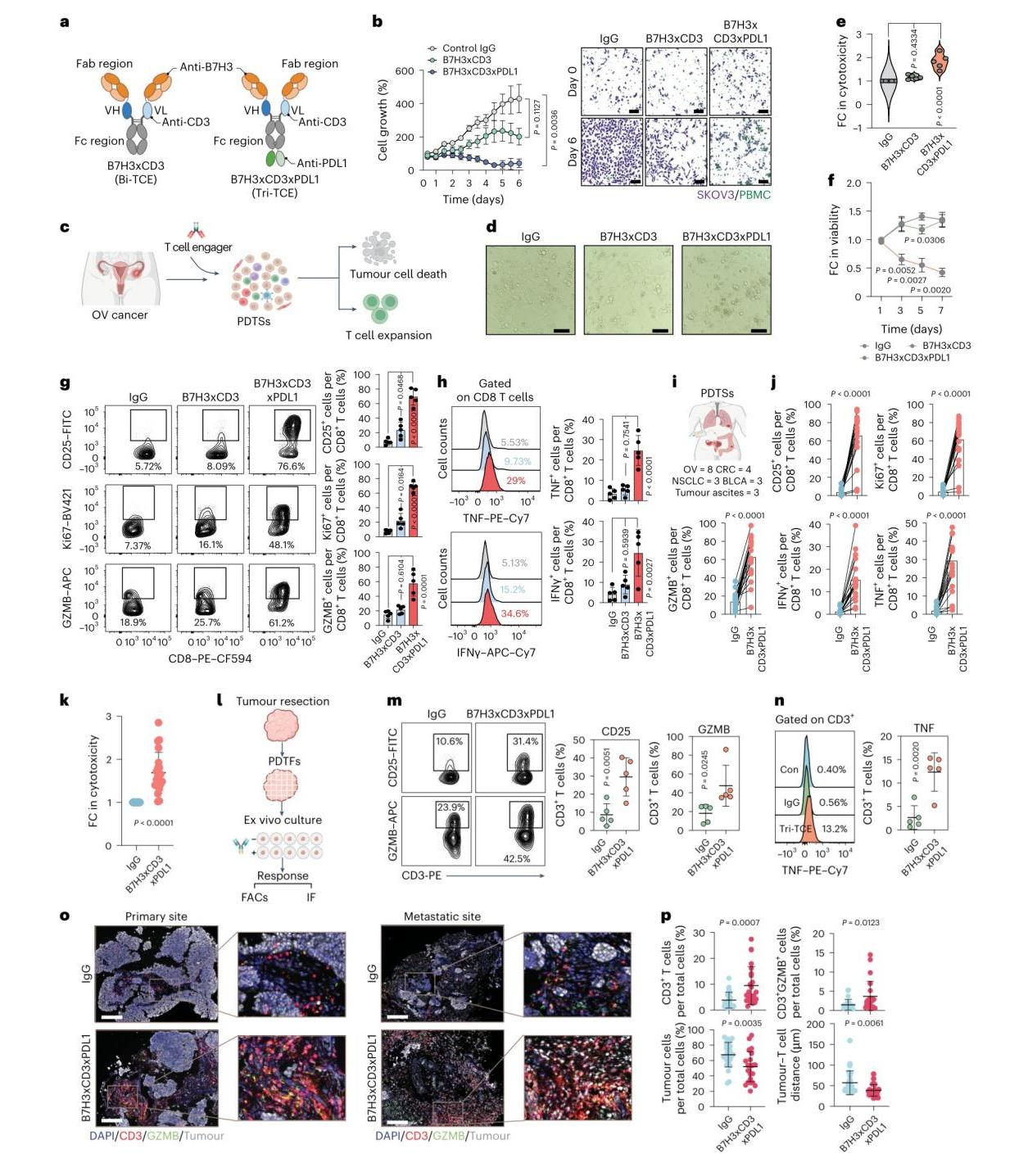
图2:双特异性/三特异性T细胞衔接器在多种原代人体系统中的疗效评估
关键作用机制:IFNγ-IL-15正反馈环路
1.精准激活T细胞:抗体同时结合肿瘤细胞B7H3和T细胞CD3,构建"免疫突触",将原本无肿瘤识别能力的旁观者T细胞转化为细胞毒性T细胞,释放穿孔素、颗粒酶直接裂解肿瘤;
2.巨噬细胞重编程:激活的T细胞分泌IFNγ,诱导免疫抑制性巨噬细胞重编程为免疫刺激表型,高表达IL-15等促免疫因子;
3.功能持续放大:IL-15进一步促进T细胞增殖、分化为效应记忆T细胞,同时IFNγ上调巨噬细胞PDL1表达,招募更多免疫细胞进入环路,形成"激活-分泌-再激活" 的正反馈,实现"以少胜多"的抗肿瘤效应。
三、重磅数据:多模型验证强效且安全的抗肿瘤疗效
1.体外与患者样本验证:跨癌种高效杀伤肿瘤
◆共培养体系中,B7H3xCD3xPDL1的半数有效浓度(EC50)仅为双特异性抗体的1/7(94.5 ng/ml vs 691.5 ng/ml),在卵巢癌细胞系 SKOV3 中实现近完全清除;
◆涵盖卵巢癌、结直肠癌、非小细胞肺癌、膀胱癌等21例患者来源肿瘤悬液(PDTS)中,抗体显著提升CD8⁺T细胞激活标志物(CD25)、增殖标志物(Ki67)及细胞因子(IFNγ、TNF)表达,肿瘤杀伤率较双特异性抗体提升2-3倍;
◆患者来源肿瘤片段(PDTF)模型中(保留肿瘤原位微环境),功能T细胞(CD3⁺GZMB⁺)浸润量增加3倍,肿瘤细胞占比降低40%,T 细胞与肿瘤细胞平均距离从150μm 缩短至50μm。
2.人源化小鼠模型:完全清除肿瘤且安全性优异
在植入SKOV3卵巢癌细胞的人源化NOG小鼠中:
◆B7H3xCD3xPDL1治疗组肿瘤体积较对照组缩小90%以上,近半数小鼠实现完全肿瘤清除,而双特异性抗体组仅轻度抑制肿瘤生长;
◆治疗后小鼠体重稳定,肝肾功能指标正常,无明显器官毒性,也未出现严重移植物抗宿主病(GVHD);
◆在A375黑色素瘤、Detroit 562头颈部鳞癌等模型中,抗体均展现强效抗肿瘤效果,验证了跨癌种适用性。
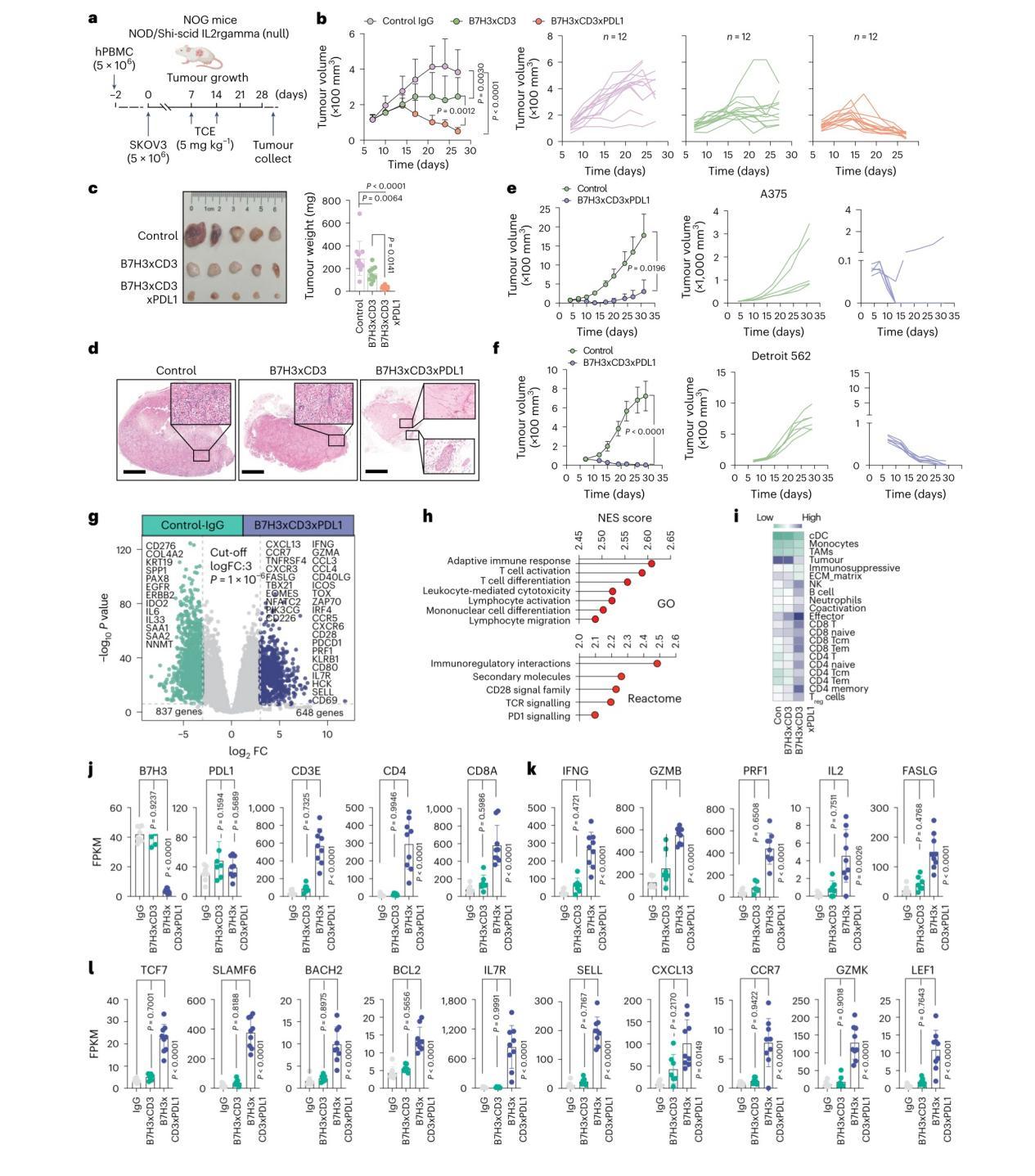
图3:B7H3xCD3xPDL1 在人源化小鼠模型中的强效抗肿瘤疗效
3.平台通用性与精准预测:助力临床转化
◆替换靶向抗原后,团队构建的HER2xCD3xPDL1、CEAxCD3xPDL1抗体同样能有效激活T细胞,抑制对应抗原阳性肿瘤生长,证明平台的通用性;
◆基于33例患者样本的转录组数据和体外药效结果,团队训练机器学习预测模型,通过识别特定免疫细胞状态(如CD8⁺细胞毒性T细胞、记忆T细胞丰度),预测患者响应率的AUC达0.94,可为临床精准筛选患者提供工具。
四、国际认可与研究意义:开创免疫治疗新方向
西班牙知名免疫学家Pedro Berraondo等在同期述评中指出,该研究以三特异性抗体创造性整合肿瘤识别与髓系细胞调控,提出了突破实体瘤免疫抑制的全新工程化范式,凸显其在下一代肿瘤免疫治疗中的重要地位。
➱这项研究的核心意义在于:
1.破解"冷肿瘤" 治疗瓶颈:首次实现旁观者T细胞激活与免疫微环境重塑的协同作用,为缺乏肿瘤特异性T细胞的实体瘤提供有效治疗策略;
2.提升治疗安全性与有效性:低亲和力CD3结合域设计减少脱靶效应,局部正反馈环路避免系统性细胞因子风暴,临床转化潜力高;
3.推动精准免疫治疗:建立的机器学习模型可快速筛选获益患者,避免无效治疗,降低医疗负担。
目前,该系列三特异性抗体已具备进入临床研究的基础,未来有望为卵巢癌、结直肠癌、膀胱癌等多种实体瘤患者,尤其是对ICIs耐药的患者,带来新的生存希望。狄文教授团队的这项成果,不仅彰显了中国学者在肿瘤免疫治疗领域的原创实力,更为全球实体瘤治疗难题提供了中国方案
专家简介
狄文 教授

上海交通大学医学院附属仁济医院
上海交通大学医学院附属仁济医院主任医师,教授,博导,上海市妇科肿瘤重点实验室主任
❖中国医师协会妇产科医师分会会长,
❖中华医学会妇产科学分会副主任委员,
❖上海市医师协会妇产科医师分会会长,
❖上海市母婴安全专家委员会主任委员,
❖《中华妇产科杂志》副总编辑,《中国实用妇科与产科杂志》和《上海医学》副主编以及多个杂志的编委。
❖担任《妇产科学》(八年制第四版)、国家卫健委住培规划教材《妇产科学》、国家卫计委英文版规划教材《妇产科学》等多本教材主编。
❖第一完成人获2010年教育部科技进步二等奖、2022年中华医学科技奖二等奖、2022年上海市科学技术奖一等奖、2018年上海医学科技奖一等奖、2009年上海医学奖二等奖及2009年上海科技进步三等奖。
❖所编教材荣获2009年上海交通大学第十二届优秀教材特等奖、2011年上海市高校优秀教材二等奖、2015年上海普通高校优秀教材奖。
❖2008年入选上海市科委优秀学科带头人培养计划、2011年获上海市领军人物。
❖2019年获中央文明办和国家卫健委“中国好医生”人物称号,2023年获世界华人医师协会“世界杰出华人医师霍英东奖”。
责编:霍盼
内容审核:狄文教授团队