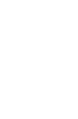子宫肌瘤的治疗有不同的选择方式。多数情况下,药物治疗是保留生育能力和避免手术的一线治疗方法,对患者来说是一个非常满意的解决方案。除此之外,手术前可以通过药物治疗减少肌瘤的体积或提高血红蛋白水平,从而尽量减少术中并发症。
在决定应该使用哪种制剂之前,必须确定是否有必要进行治疗。大多数患有子宫肌瘤的妇女是无症状的,因此不需要干预。其中约30%的人会出现症状,包括子宫异常出血、贫血、盆腔疼痛和压迫感、背痛、尿频、便秘或不孕症,需要干预治疗方案除预期治疗效果外,还取决于患者的个人治疗。每种疗法都有其自身的优点和缺点,并以不同的方式改善肌瘤体积、疼痛、月经出血和/或贫血(表1)。
PART 02 医疗方案
01 氨甲环酸
氨甲环酸(TXA)用于治疗子宫肌瘤引起的异常出血是一个合适的选择。TXA是一种合成的类似赖氨酸的抗纤溶药物,因此不是子宫肌瘤的因果治疗。通过抑制纤维蛋白溶解,有助于控制出血,但不影响肌瘤的大小。
氨甲环酸(TXA)已显示出能使子宫肌瘤患者的月经出血量平均减少89ml。有研究表明,对于月经过多的患者,其出血量可减少40%–50%。与安慰剂、非甾体抗炎药、口服孕激素、酚磺乙胺或草药相比,氨甲环酸在治疗月经过多方面似乎更为有效,但可能不如左炔诺孕酮宫内释放系统有效。在大型子宫肌瘤切除术的术中静脉输注氨甲环酸,与安慰剂相比未显示出显著差异。
TXA可在月经期间静脉注射或口服。
与TXA相关的不良反应有胃肠道不良反应、腹部不适、头痛、头晕、乳房压痛、痛经、体重变化和情绪波动。使用TXA没有血栓栓塞事件的报道。除对氨甲环酸(TXA)已知过敏外,禁忌证还包括有静脉或动脉血栓栓塞病史或活动性血栓栓塞疾病。
02 孕激素
局部用药-左炔诺孕酮宫内释放系统
左炔诺孕酮释放宫内释放系统(LNG-IUS)是一种T形装置,它将左炔诺孕酮(一种孕酮的合成衍生物)释放到子宫,最初是为了避孕。2009年,美国食品和药物管理局(FDA)也批准了这种宫内节育器的附加用途,用于治疗月经大量出血。
一项前瞻性对照研究调查了左炔诺孕酮宫内节育系统(LNG-IUS)在患有肌瘤相关重度月经过多女性中的使用效果。在放置LNG-IUS后的1个月内,Pictorial失血评估图表评分下降了86.8%(P<0.0001)。在3、12、24、36、48个月时,月经出血量分别减少92.1%、97.4%、97.4%、99.5%、99.5%。子宫平均体积明显减小,但肌瘤体积减小无统计学意义(P=0.409)。这些发现,以及治疗后血液血红蛋白和铁蛋白水平升高等额外信息,已在其他研究中得到证实。
目前有多种类型的LNG-IUS可供选择,其作用持续时间在3至5年之间。应告知患者存在环脱落的风险,这种风险与直径大于3cm的子宫肌瘤有关,但与肌瘤的位置无关。
全身治疗-口服孕激素类药物
口服孕激素具有不同的作用,这可能对与肌瘤相关的问题有意义。孕激素不仅能够稳定子宫内膜的脆弱状态、抑制子宫内膜生长,还能抑制血管生成。这些类固醇激素可促进雌二醇转化为活性较低的雌酮。它们能阻止排卵和卵巢类固醇生成,抑制雌激素受体的产生以及雌激素对子宫内膜的依赖性刺激,从而导致子宫内膜萎缩。总之,其具有多种减少出血的作用。在不同情况下,对出血的控制效果已得到证实。
对于有排卵性异常子宫出血的女性,周期性(从月经第5天开始,连续服用21天)或连续口服醋酸甲羟孕酮(MPA)、炔诺酮、醋酸甲地孕酮或微粒化孕酮,可控制月经周期并减少月经失血量。经过6个月的治疗,炔诺酮可使通过视觉出血评分测定的子宫出血量减少56%。
出现急性子宫异常出血的患者,大剂量孕酮(如:MPA20毫克,每日三次,连续1周,随后每日给药,连续3周)可显著减少月经出⾎量。
发表在《Cochrane图书馆》上的一篇系统综述比较了孕激素与释放孕激素的宫内节育系统在治疗子宫肌瘤方面的效果。该综述指出,左炔诺孕酮宫内节育系统(LNG-IUS)使用者报告点滴出血这一不良事件的可能性(64.3%)高于服用醋酸炔诺酮的女性(30%)。基于所回顾的数据,作者得出结论:目前仅有低质量证据,口服孕激素的优越性仍不明确。因此,现有证据并未强烈支持将口服孕激素用于子宫肌瘤的治疗,仅在特定病例中考虑使用。
对于以月经过多为主要症状且需要避孕的女性来说,口服孕激素可能是一个不错的选择。在这些情况下,口服孕激素具有多种益处。与其他医疗方案相比,它们性价比高,严重不良反应较少,并且被批准用于避孕。不过,需要记住的是,口服孕激素并不会减小肌瘤的体积。
03 雌激素-孕激素避孕药
复方口服避孕药(COCs)由一种雌激素和一种孕激素组成,是单片制剂,用于避孕。如今,这些药物具有更广泛的作用,可用于治疗多种病症,包括子宫肌瘤的治疗。
复方口服避孕药(COCs)可减少子宫肌瘤女性的异常子宫出血,采用碱性血红蛋白法测量,减少量为9.9ml(减少13.4%);采用图表式失血评估量表测量,减少53.5%。一项评估复方口服避孕药与肌瘤生长相关性的研究的荟萃分析显示,当前使用者肌瘤生长的风险降低了17%,不过作者指出纳入的试验之间存在显著的异质性。没有证据表明复方口服避孕药会促进子宫肌瘤生长。
现有数据表明,COCs可能是子宫肌瘤相关月经过多妇女的一种治疗选择。然而,关于其对其他肌瘤相关症状的疗效的证据有限,特别是因为COCs不能显著缩小肌瘤体积。另一个需要考虑的重要因素是患者的年龄。子宫肌瘤通常随着年龄的增长而增长,这意味着这些症状经常在生育后期出现。COCs在老年妇女中的使用仍然是一个有争议的话题。在这种情况下,建议考虑较低剂量雌激素和孕激素,以尽量减少血栓或心血管事件的风险。此外,35岁以上吸烟的妇女不应使用COCs,因为这会增加发生严重并发症的风险。总之,COCs不是子宫肌瘤的常用治疗策略,特别是在老年患者中。
文献综述评估激素替代治疗(HRT)对绝经后子宫肌瘤妇女的影响。现有资料表明,子宫肌瘤可能受到HRT的影响,但不意味着绝对禁忌证。使用HRT的子宫肌瘤妇女应定期检查,如果肌瘤出现增大,应停止激素治疗。
04 促性腺激素释放激素类似物
促性腺激素释放激素激动剂
促性腺激素释放激素(GnRH)激动剂是一类肽类物质,其结构与GnRH相似,通过氨基酸取代增强了与受体的结合亲和力。这会引起持续刺激,起初会使促性腺激素的释放增加(点火效应),这种效应可持续1-2周,之后性腺类固醇会下降,直至达到药物去势水平。
促性腺激素释放激素激动剂能有效缩小肌瘤体积(约为初始体积的50%)。多项随机、安慰剂对照研究表明,醋酸亮丙瑞林可显著减小子宫和肌瘤的体积。这有助于改善肌瘤相关症状。遗憾的是,这种高效疗法持续时间因不良反应而受到限制。其使用时间被限制在3至6个月,且停止治疗后,肌瘤会恢复到治疗前的大小。因此,GnRH类似物疗法不适合作为长期治疗手段——尽管它在术前能带来显著益处——除非与“反向添加”激素联合使用。低剂量的“反向添加”激素不会影响该疗法在缓解症状方面的效果,但能将长期不良反应降至最低。
关于术前使用促性腺激素释放激素(GnRH)类似物,术前使用GnRH激动剂与术前血红蛋白水平升高以及子宫和肌瘤体积缩小有关。然而,这些效果的代价是不良事件发生的可能性(几率)增加,特别是潮热、头痛、头晕、阴道炎、乳房大小变化和出汗。2017年发表的一项Cochrane系统综述显示了子宫切除期间及之后的这些主要结果。其他益处包括:显著减少出血量和输血需求、需要纵切口的几率降低、手术困难的可能性(几率)减小以及术后血红蛋白水平提高。在接受肌瘤切除术的女性中,大多数试验发现GnRH激动剂减少了术中出血量,但没有证据表明术前治疗会影响手术持续时间、术中输血几率、住院时间、肌瘤复发率或术后血红蛋白水平。
2020年发表的一项荟萃分析,包括213名进行宫腔镜子宫肌瘤切除术的妇女,与对照组相比,使用GnRH激动剂完全切除黏膜下肌瘤没有统计学意义(相对风险[RR]0.94, 95%可信区间[CI] 0.80-1.11);手术时间(平均差异[MD]-3.81, 95%CI-3.81至2.13);液体吸收(MD-65.90, 95%CI-9.75至2.13);或并发症(RR0.92, 95%CI 0.18-4.82),因此作者不建议在这些病例中术前常规使用GnRH激动剂。
由此产生的低雌激素血症可能会引发多种并发症,如潮热、阴道干燥、骨量受影响等。因此,促性腺激素释放激素类似物不应长期使用。作为替代方案,可以采用辅助替代治疗或添加回补策略。一项Cochrane研究表明,替勃龙、雷洛昔芬、雌三醇和依普黄酮有助于维持骨密度,而甲羟孕酮和替勃龙能够减轻血管舒缩症状。一些所用药物,如甲羟孕酮、替勃龙和结合雌激素,会产生子宫体积增大这一不良事件。
促性腺激素释放激素拮抗剂
了解子宫肌瘤生长的病理生理学后,消除促性腺激素释放激素(GnRH)刺激成为一种替代性药物治疗方案。GnRH拮抗剂可与GnRH受体可逆性结合,且不会刺激这些受体,因此不会产生突发效应,在给药后24~72小时内即可达到药物去势水平。
一项系统综述和荟萃分析评估了口服促性腺激素释放激素(GnRH)拮抗剂的应用。结果显示,600mg、400mg和200mg剂量的恶拉戈利在抑制出血方面均有效,且在不进行反向添加治疗的情况下,剂量越高,闭经的可能性越大。在未采用辅助替代治疗的方案中,子宫体积的变化更为显著。所有治疗方案均与生活质量评分的改善相关。在针对月经过多女性的随机对照实验中,也证实了子宫肌瘤女性的月经失血量能显著减少。因此,美国食品药品监督管理局(FDA)批准恶拉戈利联合雌二醇和炔诺酮用于治疗与子宫肌瘤相关的月经过多。
促性腺激素释放激素拮抗剂林扎戈利已在欧盟获批,用于治疗育龄成年女性的中重度子宫肌瘤症状。它是一种口服药物,需每日服用一次。其获批依据是Ⅲ期临床试验(PRIMROSE试验),该试验表明,它能显著减少月经过多以及与子宫肌瘤相关的症状,且具有良好的安全性。林扎戈利可以联合或不联合反向添加疗法使用。
2019年发表的一项研究比较了拮抗剂瑞卢戈利(每日口服40mg)与激动剂亮丙瑞林(每月注射1.88mg或3.75mg)。研究结果发现,两组在肌瘤大小的缩小、子宫体积的减小以及血红蛋白水平的升高方面效果相当。与亮丙瑞林相比,瑞卢戈利对月经出血的作用出现得更早,且总体耐受性良好。
一种含有40mg瑞卢戈利、1mg雌二醇和0.5mg醋酸炔诺酮的药物已在欧盟和美国获批,用于治疗与子宫肌瘤相关的月经过多。该药物需在月经周期的前5天开始,于每天大致相同的时间口服,持续服用直至绝经。这种疗法一个特别吸引人的地方是,反向添加疗法直接融入了治疗方案中。有研究表明,使用该药物2年不会导致明显的骨量流失。LIBERTY试验对这种联合疗法的效果进行了研究。与接受安慰剂治疗的女性相比,接受该疗法的女性其症状严重程度显著降低。瑞卢戈利联合疗法能大幅减少子宫肌瘤女性的月经过多症状,减轻疼痛,还能缓解与出血和盆腔不适相关的困扰。
05 孕激素受体调节剂
药物治疗的另一种可能性是使用选择性孕激素受体调节剂 (SPRM)。孕酮在子宫肌瘤发病机制中的重要性解释了SPRM治疗的有效性。临床和生化证据表明,SPRMs可以减少肌瘤的生长并改善症状。
一项Cochrane综述和荟萃分析评估了三种选择性孕激素受体调节剂(SPRM):米非司酮、醋酸乌利司他和阿索司酮。将这些药物与安慰剂进行比较后发现,选择性孕激素受体调节剂除了能减少月经出血量和提高闭经率外,还能改善肌瘤症状的严重程度和生活质量。他们还将选择性孕激素受体调节剂与醋酸亮丙瑞林进行了比较,未发现有证据表明两组在改善生活质量和盆腔疼痛方面存在差异。关于不良反应,选择性孕激素受体调节剂会导致子宫内膜发生良性变化,这种变化与癌症无关,也不是癌前病变。
醋酸乌利司他已被证实是治疗月经过多的一种有效的药物治疗选择,但由于出现了一些严重肝损伤病例,目前其使用受到严格限制。在人们知晓醋酸乌利司他可能引发的肝脏并发症之前,该药物被视为子宫肌瘤治疗领域的一项突破。PEARL研究表明,在醋酸乌利司他治疗期间,能够有效控制因子宫肌瘤导致的过度出血,并缩小肌瘤体积。基于这些研究结果,这种疗法在全球范围内被广泛采用,直到有关不良反应的报告出现。导致醋酸乌利司他发布安全警告的主要并发症是严重肝损伤的发生,其中包括需要进行肝移植的急性肝衰竭病例。目前尚无法识别出肝损伤风险增加的患者。因此,醋酸乌利司他的使用受到了严格限制。如今在欧洲,该药物仅在特定条件下且需定期监测肝功能的情况下才被批准使用。在美国,由于这些安全顾虑,醋酸乌利司他未被批准用于子宫肌瘤的治疗。
一项研究评估了宫腔镜子宫肌瘤切除术前2个月使用醋酸乌利司他的影响研究显示,与术前未接受药物治疗的患者相比,接受这种术前管理的患者手术时间明显缩短,液体吸收明显减少(表2)。
PART 03 全球可及性
我们所呈现的关于子宫肌瘤药物疗法的大部分临床证据,主要来自于高收入地区(如美国和欧洲)开展的研究。其在中低收入国家的应用经验较为有限。
新兴且高成本的疗法,包括促性腺激素释放激素拮抗剂(如瑞卢戈利)和选择性孕激素受体调节剂(如醋酸乌利司他),往往面临监管和经济方面的障碍,这限制了它们在资源有限地区的使用。据作者所知,正因如此,在亚洲和非洲的许多地区,人们无法全面且公平地获得这些药物。相比之下,在高收入的亚洲国家,像瑞卢戈利这类药物已被批准用于治疗子宫肌瘤。在许多中低收入国家,尽管口服孕激素和氨甲环酸在缩小肌瘤体积方面的疗效有限,但由于价格更为低廉,它们仍是药物治疗的主要选择。开发具有成本效益且安全的治疗对于实现医疗公平至关重要。
PART 04 未来选择
由于子宫肌瘤是一种极为常见的疾病,预计未来会有更多关于其药物治疗的研究。在瑞卢戈利和林扎戈利取得成功后,促性腺激素释放激素(GnRH)拮抗剂类新疗法可能会成为一种选择。例如,据我们所知,目前在中国北京正在开展一项针对患有子宫肌瘤合并月经过多患者的Ⅲ期临床试验,试验药物为SHR7280,该试验正在招募受试者。
此外,还有多项研究在探讨维生素和其他膳食补充剂作为子宫肌瘤辅助治疗的应用。这些研究进展颇具意义,因为它们未来可能会提供具有成本效益且低风险的治疗替代方案。
PART 05 结论
药物治疗是子宫肌瘤管理中的关键组成部分。治疗药物的选择取决于患者的主要症状和整体临床情况。多种药物(包括激素类和非激素类药物)可用于子宫肌瘤的管理,以控制症状并提高生活质量。然而,仅有少数药物获得了针对该适应症的正式监管批准。这些药物在全球范围内的可及性仍然有限,找到更具(成本)效益的治疗方法仍是一个值得追求的目标。
【文献参考】
1. Angioni S, D'Alterio MN, Daniilidis A. Highlights on medical treatment of uterine fibroids. Curr Pharm Des. 2021;27(36):3821-3832.
2. Giuliani E, As-Sanie S, Marsh EE. Epidemiology and management of uterine fibroids. Int J Gynaecol Obstet. 2020;149(1):3-9.
3. Sohn GS, Cho S, Kim YM, Cho CH, Kim MR, Lee SR. Current medical treatment of uterine fibroids. Obstet Gynecol Sci. 2018;61(2):192-201.
4. Ng W, Jerath A, Wąsowicz M. Tranexamic acid: a clinical review. Anaesthesiol Intensive Ther. 2015;47(4):339-350.
5. Eder S, Baker J, Gersten J, Mabey RG, Adomako TL. Efficacy and safety of oral tranexamic acid in women with heavy menstrual bleeding and fibroids. Womens Health (Lond). 2013;9(4):397-403.
6. Bryant-Smith AC, Lethaby A, Farquhar C, Hickey M. Antifibrinolytics for heavy menstrual bleeding. Cochrane Database Syst Rev. 2018;4(4):CD000249.
7. Barbosa PA, Villaescusa M, Andres MP, Fernandes LFC, Abrão MS. How to minimize bleeding in laparoscopic myomectomy. Curr Opin Obstet Gynecol. 2021;33(4):255-261.
8. Abdou AM, Eldesouky E, Farag E, et al. Oxytocin versus a combination of tranexamic acid and ethamsylate in reducing intraoperative bleeding during abdominal myomectomy: a randomized clinical trial. BMC Womens Health. 2023;23(1):398.
9. Chauncey JM, Wieters JS. Tranexamic acid. StatPearls. StatPearls Publishing; 2023.
10. Islam MS, Protic O, Giannubilo SR, et al. Uterine leiomyoma: available medical treatments and new possible therapeutic options. J Clin Endocrinol Metab. 2013;98(3):921-934.
11. Kriplani A, Awasthi D, Kulshrestha V, Agarwal N. Efficacy of the levonorgestrel-releasing intrauterine system in uterine leiomyoma. Int J Gynaecol Obstet. 2012;116(1):35-38.
12. Socolov D, Blidaru I, Tamba B, Miron N, Boiculese L, Socolov R. Levonorgestrel-releasing intrauterine system for the treatment of menorrhagia and/or frequent irregular uterine bleeding associated with uterine leiomyoma. Eur J Contracept Reprod Health Care. 2011;16(6):480-487.
13. Jiang W, Shen Q, Chen M, et al. Levonorgestrel-releasing intrauterine system use in premenopausal women with symptomatic uterine leiomyoma: a systematic review. Steroids. 2014;86:69-78.
14. Bradley LD, Gueye NA. The medical management of abnormal uterine bleeding in reproductive-aged women. Am J Obstet Gynecol. 2016;214(1):31-44.
15. Tosun AK, Tosun I, Suer N. Comparison of levonorgestrel-releasing intrauterine device with oral progestins in heavy menstrual bleeding (HMB) cases with uterine leiomyoma (LNG-IUD and oral progestin usage in myoma uteri). Pak J Med Sci. 2014;30(4):834-839.
16. Munro MG, Mainor N, Basu R, Brisinger M, Barreda L. Oral medroxyprogesterone acetate and combination oral contraceptives for acute uterine bleeding: a randomized controlled trial. Obstet Gynecol. 2006;108(4):924-929.
17. Sangkomkamhang US, Lumbiganon P, Pattanittum P. Progestogens or progestogen-releasing intrauterine systems for uterine fibroids (other than preoperative medical therapy). Cochrane Database Syst Rev. 2020;11(11):CD008994.
18. Croxatto HB. Progestin implants. Steroids. 2000;65(10–11):681-685.
19. Qin J, Yang T, Kong F, Zhou Q. Oral contraceptive use and uterine leiomyoma risk: a meta-analysis based on cohort and case-control studies. Arch Gynecol Obstet. 2013;288(1):139-148.
20. Moro E, Degli Esposti E, Borghese G, et al. The impact of hormonal replacement treatment in postmenopausal women with uterine fibroids: a state-of-the-art review of the literature. Medicina (Kaunas). 2019;55(9):E482.
21. Faculty of Sexual and Reproductive Healthcare (FSRH). Contraception for Women Aged over 40 Years. FSRH Guideline. August 2017 [amended July 2023]. NICE accredited. FSRH; 2023.
22. Ascoli M, Puett D. The gonadotropin hormones and their receptors. In: Strauss JF, Barbieri RL, eds. Yen & Jaffe's Reproductive Endocrinology: Expert Consult – Online and Print. 9th ed. Elsevier Inc.; 2023:35-55.
23. Caird LE, West CP, Lumsden MA, Hannan WJ, Gow SM. Medroxyprogesterone acetate with Zoladex for long-term treatment of fibroids: effects on bone density and patient acceptability. Hum Reprod. 1997;12(3):436-440.
24. Lethaby A, Puscasiu L, Vollenhoven B. Preoperative medical therapy before surgery for uterine fibroids. Cochrane Database Syst Rev. 2017;11(11):CD000547.
25. Corrêa TD, Caetano IM, Saraiva PHT, Noviello MB, Santos Filho AS. Use of GnRH analogues in the reduction of submucous fibroid for surgical hysteroscopy: a systematic review and meta-analysis. Rev Bras Ginecol Obstet. 2020;42(10):649-658.
26. Donnez J, Dolmans MM. Uterine fibroid management: from the present to the future. Hum Reprod Update. 2016;22(6):665-686.
27. Moroni RM, Martins WP, Ferriani RA, et al. Add-back therapy with GnRH analogues for uterine fibroids. Cochrane Database Syst Rev. 2015;2015(3):CD010854
28. Telek SB, Gurbuz Z, Kalafat E, Ata B. Oral gonadotropin-releasing hormone antagonists in the treatment of uterine myomas: a systematic review and network meta-analysis of efficacy parameters and adverse effects. J Minim Invasive Gynecol. 2022;29(5):613-625.
29. Carr BR, Steward EA, Archer DF, et al. Elagolix alone or with add-back therapy in women with heavy menstrual bleeding and uterine leiomyomas: a randomized controlled trial. Obstet Gynecol. 2020;136(5):893-903.
30.www.fda.gov/news-events/press-announcements/fda-approves-new-option-treat-heavy-menstrual-bleeding-associated-fibroids-women
31. Donnez J, Taylor HS, Stewart EA, et al. Linzagolix with and without hormonal add-back therapy for the treatment of symptomatic uterine fibroids: two randomised, placebo-controlled, phase 3 trials. Lancet. 2022;400(10356):896-907.
32. Donnez J, Becker CM, Mangler M, et al. Linzagolix rapidly reduces heavy menstrual bleeding in women with uterine fibroids: an analysis of the PRIMROSE 1 and 2 trials. Fertil Steril. 2025;123(6):1093-1100.
33. Dababou S, Garzon S, Laganà AS, et al. Linzagolix: a new GnRHantagonist under investigation for the treatment of endometriosis and uterine myomas. Expert Opin Investig Drugs. 2021;30(9):903-911.
34. Osuga Y, Enya K, Kudou K, Tanimoto M, Hoshiai H. Oral gonadotropin-releasing hormone antagonist relugolix compared with leuprorelin injections for uterine leiomyomas: a randomized controlled trial. Obstet Gynecol. 2019;133(3):423-433.
35. Syed YY. Relugolix/estradiol/norethisterone (norethindrone) acetate: a review in symptomatic uterine fibroids. Drugs. 2022;82(17):1549-1556.
36. www.ema.europa.eu/en/medicines/human/EPAR/ryeqo
37. Stewart EA, Lukes AS, Venturella R, et al. Quality of life with relugolix combination therapy for uterine fibroids: LIBERTY randomized trials. Am J Obstet Gynecol. 2023;228(3):320.e1-320.e11.
38. Al-Hendy A, Lukes AS, Poindexter AN 3rd, et al. Treatment of uterine fibroid symptoms with Relugolix combination therapy. N Engl J Med. 2021;384(7):630-642.
39. Wrona W, Stępniak A, Czuczwar P. The role of levonorgestrel intrauterine systems in the treatment of symptomatic fibroids. Prz Menopauzalny. 2017;16(4):129-132.
40. Donnez J, Tatarchuk TF, Bouchard P, et al. Ulipristal acetate versus placebo for fibroid treatment before surgery. N Engl J Med. 2012;366(5):409-420.
41. European Medicines Agency. Ulipristal Acetate for Uterine Fibroids: EMA Recommends Restricting Use [Internet]. EMA; 2020 [cited 2025 Aug 3]. https://www.ema.europa.eu/en/news/ulipristal-acetateuterine-fibroids-ema-recommends-restricting-use
42. Vitale SG, Ferrero S, Caruso S, et al. Ulipristal acetate before hysteroscopic myomectomy: a systematic review. Obstet Gynecol Surv. 2020;75(2):127-135.
43. Hengrui Therapeutics Inc. A Phase II/III Study of Efficacy and Safety of SHR7280 Tablets in Subjects With Menorrhagia With Uterine Fibroids. ClinicalTrials.gov [Internet]. Identifier NCT05442827 [cited 2025 Aug 6]. https://clinicaltrials.gov/study/NCT05442827?cond=Uterine%20Fibroids&intr=Medication&aggFilters=status:rec%20act&rank=10
<上下滑动查看>
审校专家简介

周金华教授
主任医师,教授,博士生导师,博士后合作导师
苏州大学附属第一医院妇产科 科副主任医学博士, MD. Anderson癌症中心博士后
❖中华医学会妇科肿瘤分会 青年学组成员
❖苏州市医学会妇产科分会 副主任委员
❖苏州市妇科医疗质控中心 副主任
❖江苏省研究型医院学会妇科肿瘤专业委员会 副主任委员
❖江苏省抗癌协会妇科肿瘤分会青委会 副主任委员
❖第十版《妇产科学》(人卫版)数字编委
❖江苏省“333人才工程”培养对象
❖江苏省妇幼健康重点人才
❖江苏省青年医学重点人才
先后主持国家自然科学基金项目4项,第一/通讯作者(含共同)发表SCI论文二十余篇,影响因子累计超180分,10分以上5篇,获国家发明专利一项,先后获全国妇幼健康自然科学奖、江苏省科学技术奖、江苏省医学科技奖等奖项
译者简介

施秀
苏州大学附属第一医院
苏州大学附属第一医院妇产科副主任医师,副教授
❖医学博士,在站博士后,硕士研究生导师,苏州市卫生青年骨干人才
❖德国杜塞尔多夫大学医院访问学者
❖江苏省研究型医院学会妇科肿瘤专业委员会委员兼秘书
❖江苏省医学会妇产科学分会青年学组委员
❖江苏省抗癌协会妇科肿瘤专委会整合康复学组委员
❖苏州市医学会妇产科学分会青年委员会副主任委员
❖苏州市妇科专业医疗质量控制中心秘书
❖主持国自然青年基金、苏州市科技创新计划等科研项目
❖获江苏省第二十一次妇产科学学术会议论文一等奖
❖获江苏省医学科技二等奖、江苏省医学新技术引进二等奖
图文来源:Diaz I,Lumsden MA,Zeppernick M. 子宫肌瘤的医学治疗:国际妇产科联盟最佳实践指南. 国际妇产科杂志. 2025;171:507-512. doi:10.1002/ijgo . 70497
责编:霍盼