欧洲妇科肿瘤学会(ESGO)、国际外阴阴道疾病研究学会(ISSVD)、欧洲外阴疾病研究学会(ECSVD)和欧洲阴道镜检查联合会(EFC)是领先的国际社会中妇科医生、病理学家、皮肤科医生和其他相关学科的学术研究会。ECSVD、EFC、ESGO和ISSVD合作制定了关于阴道上皮内瘤变的共识声明。
2012年美国病理学家协会(College of American pathologists,CAP)和美国阴道镜检查与子宫颈病理学会(American society of colposcopy and Cervical pathology,ASCCP)联合发布了下生殖道和肛门鳞状上皮病变术语(Lower anogenital squamous terminology,LAST),LAST命名的提出,对于包括子宫颈、阴道、外阴等女性下生殖道在内的所有HPV感染相关的鳞状上皮病变均推荐采用鳞状上皮内病变(Squamous intraepithelial lesion,SIL),并且将其分为两级,即低级别鳞状上皮内病变(Low‑grade squamous intraepithelial lesion,LSIL)和高级别鳞状上皮内病变(High-grade squamous intraepithelial lesion,HSIL)。
2020世界卫生组织(Word health organization,WHO)发布的第5版WHO分类仍采用LSIL和HSIL 两级分类法,在子宫颈及阴道鳞状上皮病变中提出CINⅠ和VaINⅠ是LSIL的同义词,而HSIL的同义词则包括CIN 2和CIN 3及VaIN 2和VaIN 3。
2011年(International federation for cervical pathology and colposcopy ,IFCPC)发布了第一个阴道镜术语(见表1),其诊断的可靠性在69.2%至82.5%之间。为提高诊断的准确性,建议绝经后妇女接受局部雌激素治疗,以区别良性萎缩性改变和癌前病变。

VaIN(阴道SIL)是一种罕见的实体组织病变,仅占女性下生殖道癌前病变的0.4%。发病率为0.2-2例/每10万妇女/年。它的发生率大约是宫颈上皮内瘤变(宫颈CIN/SIL)的100倍。尽管阴道癌的发病率相对稳定,但癌前病变的发病率似乎有所增加。这可能是与筛查方法的改进以及对该疾病认识的提高有关。
高级别VaIN的发病率与年龄有关,随着年龄的增长而增加,直到70-79岁(1.5例/每10万女性/年)之后略有下降。阴道高级别病变(VaIN 2/3;HSIL)的发生率相对稳定,但可接种HPV疫苗后,在最年轻群体(<30岁)中,其发生率下降了近16%。
VaIN(阴道SIL)是大多数HPV感染相关阴道癌的前兆。据报道VaIN向鳞状细胞癌的进展率在2%至7%。阴道的低级别病变(VaIN 1;阴道LSIL)与低危型和高危型的HPV感染相关。在阴道高级别病变(VaIN 2/3;阴道HSIL)中,最常见的HPV基因型是:HPV 16、HPV 33和HPV 45。吸烟、免疫抑制、艾滋病毒感染、宫颈HSIL病史是持续性HPV感染的高危因素,亦增加了发生阴道癌前病变和浸润癌的风险。
有其他恶性肿瘤盆腔放疗史的人群发生阴道癌前病变或阴道癌的风险亦增加。根据目前的研究,尚未发现与遗传性阴道癌相关的基因突变。遗传因素可能影响宫颈高危型HPV(hr-HPV)感染的易感性。目前研究认为甲基化基因(细胞粘附分子1的CpG位点,CADM1)、T淋巴细胞成熟相关蛋白(MAL)和microRNA124-2(miR124-2)似是与HPV相关CIN有关的生物标志物。
阴道微生物群的稳定性和组成对宿主先天免疫反应和对包括HPV在内的感染的易感性方面起着重要作用。乳酸杆菌种类的减少与hr-HPV感染相关,且随着疾病严重程度的增加,其相关性上升。另外,乳酸杆菌的减少与CIN的进展或消退有关。阴道微生物的变化与HPV协同作用导致疾病发生,其潜在机制是改变阴道pH、产生细菌素、破坏黏膜上皮细胞的完整性、氧化应激及对p53、pRB和生存素等细胞受体的影响。
VaIN无特异性的临床表现,通常无明显症状,且肉眼难以观察,多为筛查宫颈病变或既往宫颈病变治疗随诊时发现。
VaIN发生的高危人群有:
1.有宫颈癌或宫颈HSIL病史者。
2.因宫颈HSIL行子宫切除术者。
3.既往曾接受过妇科恶性肿瘤放疗者。
4.免疫抑制者。
5.绝经者。
6.己烯雌酚(DES)暴露的患者。
细胞学检查的敏感性为67.5–76.2%,在筛查阴道病变时比阴道镜检查更为可靠。当与hr-HPV检测联合时,可将准确率提高至95%。
阴道病变肉眼难以察觉,阴道镜检查是必须的。除了需行醋酸试验及Lugol’s碘染色 (Schiller’s test),检查时必须保证阴道壁和褶皱的完全可视化,因为病变可藏匿其中(见图1)。应用醋酸后,阴道HSIL通常呈白色,边缘尖锐,表面呈颗粒状。偶尔,可以看到点状血管。很少发现镶嵌或角化样改变(见图2)。当出现不典型血管和脆弱血管,病变不规则、表面溃疡,则可疑癌变(见图3)。VaIN表现为Schiller’s test阴性(见图4),对于阴道黏膜明显萎缩的绝经妇女,进行Schiller’s test前建议阴道局部雌激素治疗3-4周。
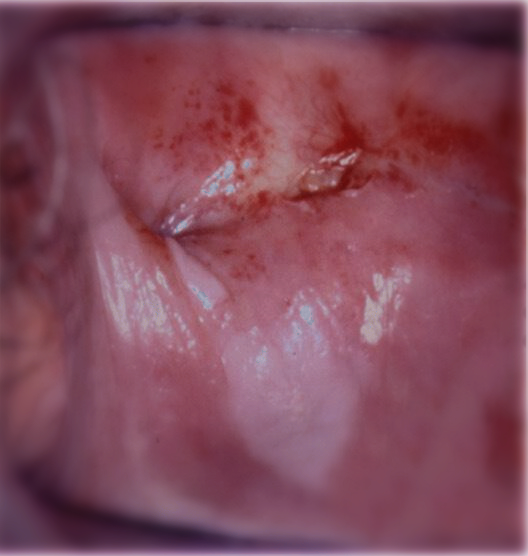
图1 阴道后壁和阴道断端褶皱之间的VaIN3(阴道HSIL)
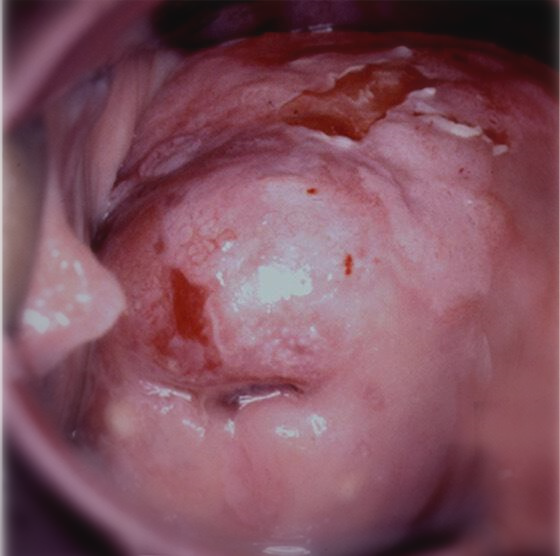
图2 CIN3(宫颈HSIL)(延伸至阴道前壁(VaIN3/阴道HSIL)
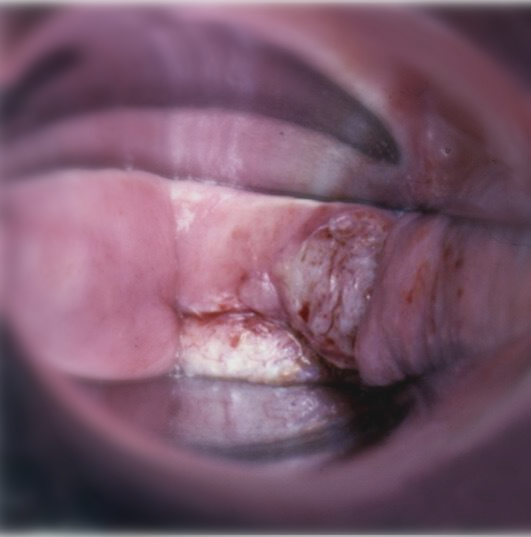
图3 宫颈HSIL子宫切除术后阴道断端浸润性癌
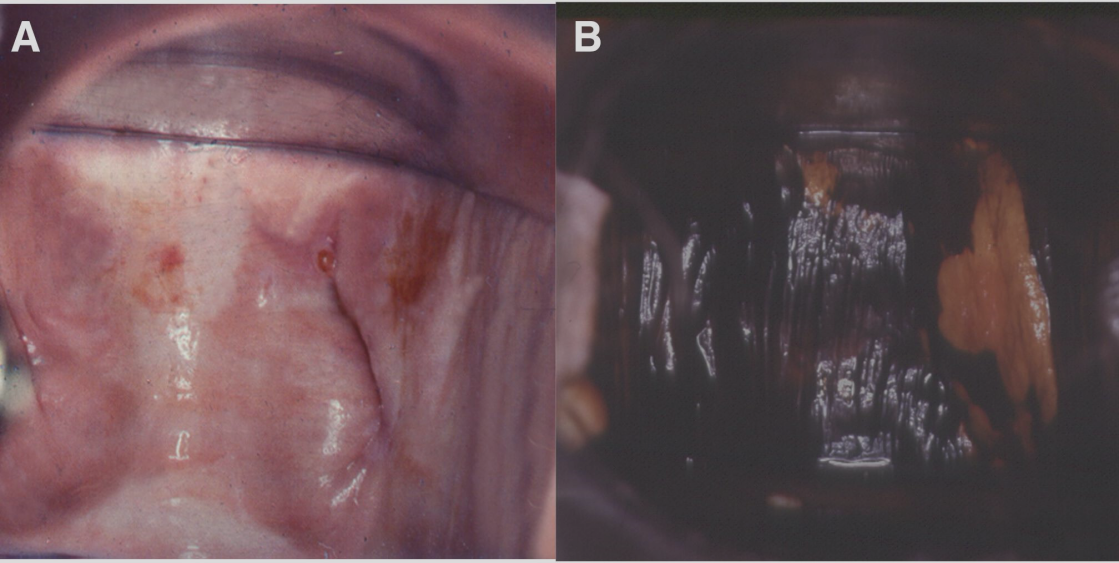
图4 应用醋酸后的VaIN3(阴道HSIL)(A),Lugol碘溶液染色后的(B)
阴道镜评估外阴病变困难的原因:
1.待检查的范围较大。
2.很难从单一的角度看到大部分的变化。
3.阴道镜下形态不如宫颈病变特异性高。
4.子宫切除术后,缝合的阴道穹窿可能不易看到。
5.癌前病变通常是多灶性的。
6.区分LSIL与真正的癌前病变(HSIL)很重要,以避免过度治疗。
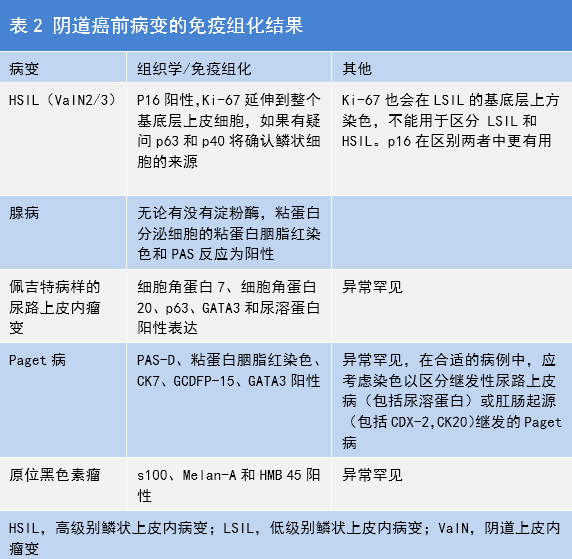
组织病理学和免疫组化是诊断不同类型的阴道癌前病变的金标准。高级别VaIN(VaIN 2/3,阴道HSIL)组织学表现为至少从基底膜向上的三分之二的鳞状上皮细胞成熟异常。P16免疫组化有助于区分VLSIL与VHSIL。Ki-67免疫组化可以区分SIL和非SIL(阴道不同类型癌前病变免疫组化详见表2)。
阴道低级别病变(HPV感染/VaIN1;阴道LSIL)被认为是HPV感染导致,但进展风险低,自发消退的可能性高。研究表明,48.8-88%的病例在未经治疗的情况下可以自发消退。有证据表明,对VaIN 1患者的治疗并不能导致更好的预后。因此,阴道低级别病变可以观察。但由于即使在接受激光治疗或切除治疗后仍存在较高的复发率(分别为24.3%和22.2%),因此需要严密随访。
阴道高级别病变(VaIN 2/3,阴道HSIL)有进展为阴道癌的风险,需要治疗。既往以根除疾病为目的的大范围手术切除和放射治疗最为常见,但严重降低了患者的生活质量。目前更趋于保守的治疗方式如局部切除、消融或药物治疗为一线治疗方式。治疗的目的是保持阴道的正常解剖结构,保持阴道的弹性、容量和延展性。
VaIN的手术干预包括手术切除(从广泛的局部切除到部分上阴道切除甚至全阴道切除)和消融手术{二氧化碳(CO2)激光汽化、超声抽吸治疗(CUSA)、光动力疗法(PDT)、电凝固疗法、等离子体能量消融等}。手术切除是首选。消融手术必须在治疗前进行病理活组织检查以排除恶性肿瘤。
广泛的局部切除术与最低的复发风险相关,切除后报告的残留病变发生率为8.6%至18.9%。但由于阴道的SIL通常是多灶性的,因此其适用性有限。VaIN手术切除的成功率较高,在66%-81%之间。在一项对35例接受广泛局部切除治疗的VaIN 3患者的研究中,23例患者(66%)患者在中位随访44个月时无疾病复发。手术的短期并发症为出血和感染,远期并发症为阴道的缩短或狭窄。
二氧化碳(CO2)激光可同时用于局部组织切除和消融。通常与其他治疗方法联合,多用于治疗多灶性疾病,常见的并发症为出血和疼痛。其破坏上皮深度可至1-1.5mm,但不破坏基底层结构。其缺点是无法治疗隐藏在阴道褶皱的病变。文献研究报道CO2激光治疗阴道高级别病变的一次的治愈率在73.5%-86%间。在一项纳入了24例VaIN 3患者的研究中,17例(70.8%)患者在一次治疗后病变完全消除,19例(79.2%)患者需要多次治疗。
部分上阴道的切除可用于治疗阴道顶端或阴道断端瘢痕处病变,对于累及阴道下1/3病变或多灶性病变,可联合CO2激光治疗。Luyten等的一项对33例VaIN 3患者行单纯激光阴道剥离术的研究中,治愈率为87%,另外两项研究报道对VaIN 3行部分(上)阴道切除术的患者的治愈率相似,分别为84%和88%。
全阴道切除术不被推荐,只在高度选择的广泛或持续性病变中应用,或某些特定情况如复发性广泛性病变或子宫切除术后阴道明显变短。
超声抽吸治疗(CUSA)是一种安全有效的治疗方式,其效果与经典手术相似。一项纳入92例VaIN患者的研究中显示,中位随访时间为4.5年后,应用CUSA治疗的治愈率约为80.4%。该手术可以精确切除表皮或粘膜病变,而不会对周围结构或潜在基底层造成热或机械损伤。CUSA是一种微创手术,需要全身或局部麻醉,且设备昂贵并需一定时间的培训。在一项涉及46例CUSA治疗复发的研究中,CUSA组(52%)未出现再次复发的比例明显高于其他治疗组(9%)(p<0.001)。
环形电切术由于难以掌握切除深度而不被推荐用于阴道疾病治疗。但有报道其用于治疗阴道前穹隆处的VaIN。一项纳入了23例组织学证实为VaIN(VaIN1-3)患者的研究中,环形电切术后12个月的完全缓解率为86.96%,而24个月的完全缓解率为75%。
光动力疗法(PDT)治疗依赖于光敏剂。光敏剂-5-氨基乙酰丙酸(ALA)可被异常细胞选择性吸收,然后被特定波长的光激活,产生单线态氧,从而杀死靶细胞。一项评估ALA-PDT治疗hr-HPV阳性的VaIN患者有效性和安全性的研究显示,疾病完全缓解率在88.64%至90.9%之间。HPV清除率为38.1%至60.98%,随访12个月时HPV清除率为67.1%。
电凝治疗亦可用于治疗阴道HSIL,能够消融深度为1.5 mm。然而,它不如激光精确。一项对184例接受局部切除联合电凝治疗的VaIN患者的回顾性研究显示疾病缓解率为87.62%。
等离子体能量消融是一种消融技术,类似于CO2激光消融术。在一项纳入了41例接受该方式治疗的外阴或阴道HSIL的患者研究中,中位随访时间29.3个月后,等离子体能量消融组和CO2激光组并发症和复发的发生率相似(4.8% vs 9%)、(33.3% vs 28.6%)。
局部应用治疗药物具有治疗整个阴道黏膜的优点,可治疗多灶性疾病和阴道褶皱内疾病。但不能到达阴道断端瘢痕内的埋藏上皮细胞。药物治疗前必须除外阴道癌的可能。
咪喹莫特是一种针对 TLR-7 的免疫反应调节剂,可刺激树突状细胞分泌促炎细胞因子,从而引发强烈的免疫浸润,并增加T细胞介导反应的有效性。Buck等的一项研究中,42例患者中有36例(86%)在完成初始治疗后疾病得以清除。随访至少6个月后,92%的患者仍未发现VaIN。一项随机临床试验的结果显示,阴道应用咪喹莫特似乎与激光治疗VaIN一样有效。咪喹莫特组80%的病例,激光组100%病例观察到组织学消退(P=0.628)。
5-氟尿嘧啶(5-FU)被认为有希望用于VaIN的局部治疗中。最常见副作用的是刺痛和性交困难。Fiascone等的一项研究中,104例VaIN患者最初接受了5-FU、切除或激光消融治疗。接受5-FU治疗的患者的治愈率最高(为74%,而后两者分别为57%和41%)。另一项纳入30例接受5-FU治疗的患者的研究显示了更高的治愈率(81-86%)。但也有研究报告称5-FU治愈率较低,约62.5%。
雌激素可能有助于VaIN的消除。Rhodesa评估了雌激素治疗作为VaIN潜在治疗方式的有效性。该研究纳入83例VaIN1-3患者,采用或不使用局部雌激素治疗,总体组织学消退率为85.5%。在40例仅接受阴道内雌激素治疗的患者中,90%的患者病变消退或治愈。另外32例(81.3%)接受阴道内雌激素治疗联合一种或多种其他治疗方式的患者病变消退或治愈,而在未接受阴道内雌激素治疗的患者中病变消退率为71.4%。
三氯乙酸是一种强大的角化溶解剂,已被证实对HPV相关的生殖器疣有治疗作用。在过去曾被用于治疗VaIN,但随着其他有效的治疗方法的出现,其已被淘汰。
近距离放射治疗是治疗方式之一,但由于有远期放射效应的风险,不建议作为一线治疗。但对于保守治疗后复发或保守手术不可行的VaIN 2/3患者可能有效。常见的剂量是60Gy,照射至阴道黏膜表面下5 mm。在一项回顾性研究中,28例VaIN患者接受了低剂量近距离放射治疗,在中位随访41个月后,仅一例复发,5年和10年的局部控制率为93%。其他研究中的无病生存率也同样很高约86.37–90%。
联合治疗:局部手术切除联合药物治疗,ALA-PDT联合CO2激光治疗等均有文献显示有一定的有效性。
VaIN复发与多项因素有关。
VaIN的初始治疗方法:一项对132例阴道HSIL患者的不同治疗方法的研究表明,切除治疗和CO2激光消融的总体治愈率相同(69%)。效果较差的是5-FU,治愈率为46%,电凝只有25%。一般来说,所有的切除方法都有相似的复发率,约7.2–20.8%。激光消融和局部切除有相似的局部复发率(18.6%/17.1%)。另外2项研究结果均显示药物治疗后的复发率高于切除手术后的复发率。
VaIN的严重程度:Lin等发现,VaIN 的严重程度是病变持续或复发的唯一显著的独立预测因子(OR3.5,95%CI1.1-11.6,p=0.038)。Kim等对576名阴道SIL患者研究后发现48.8%的阴道LSIL患者可自发消退,而阴道HSIL患者自发消退率为46.2%。接受治疗的VaIN 2/VaIN 3患者中分别有36.8%/38.5%的病例出现复发或进展,两者无显著差异。在另一项纳入131例VaIN患者的研究显示,15.26%的VaIN 3患者复发,但只有3.05%的VaIN 2患者复发。
疾病的分布:研究表明,多灶性疾病的复发率(57%)高于单灶性疾病(43%)。阴道穹窿内的HSIL(VaIN 2/3)是复发的主要危险因素。在52例接受激光消融术(28例)和上阴道切除术(24例)的患者中,治愈率分别为68%和80%。子宫切除术组的激光治疗失败率是上阴道切除术后的2倍(46% vs 20%)。
既往治疗和年龄:Yu等通过对118例VaIN患者的回顾性研究得出结论,与CIN或宫颈癌相关的VaIN以及VaIN 2/3复发和进展为浸润性癌的可能性高。Kim等在对375例接受子宫切除术的VaIN患者进行的多变量分析中,50岁以上是VaIN复发的唯一独立危险因素。
HPV持续感染:与第二次复发相关的独立变量之一是HPV 16或18的持续感染。Cho等的一项对389 例患者的回顾性研究显示:接受初始激光治疗、近距离放射治疗或阴道切除术的患者有较高的组织病理学缓解率(分别为73.7%、71.4%和100%)和相似的hr-HPV清除率(分别为52.6%、57.1%和50.0%)。
VaIN进展为浸润性阴道癌的风险不可忽视。据报道,阴道HSIL(VaIN2/3)治疗后进展为侵袭性癌风险为3.2%-5.8%,从治疗到进展的平均时间间隔为54.6-61个月。因此需长期随访。
阴道LSIL(VaIN 1)的随访,建议在12个月时进行联合检测。鉴于HPV检测的高阴性预测价值,在12个月内只需要一次联合检测。如果只使用细胞学检查,应在12个月内重复两次。如果联合检测或重复细胞学检查为阴性,无需进一步筛查。如检测呈阳性者应转诊阴道镜检查。对于既往无HSIL或癌症病史,LSIL/VaIN 1持续2年以上患者,将筛查间隔延长到每2至3年一次是合理的。
阴道高级别病变治疗后的第一次检测(VaIN 2/3)应在6个月时进行细胞学检查和HPV检查。如果在6个月和12个月的随访中,疾病完全缓解,无复发,患者应每年进行细胞学检查或每2-3年联合检测一次。在HPV检测阳性和/或细胞学异常的情况下,建议转诊阴道镜评估。阴道镜检查应该由经验丰富的阴道镜医生来做。阴道镜检查异常需要进一步活检。
持续的HPV感染,特别是HPV 16感染,与HSIL(VaIN 2/3)和阴道癌的发生有关。HPV疫苗在预防与疫苗类型相关的病变方面非常有效。鼓励戒烟,可能降低阴道HSIL的风险。
免疫抑制人群包括感染HIV的女性、接受免疫抑制药物治疗或患有自身免疫性疾病的人群。证据显示,免疫抑制是发生HPV感染相关癌前病变和浸润性癌的危险因素。HPV和HIV 具有紧密的免疫相互作用。HIV(+)的女性在年轻时的VaIN发病率较高,并且经常表现多灶性病变。HIV(+)较HIV(-)女性的复发率和进展率高。高效抗逆转录病毒治疗可能会降低VaIN,但需进一步研究。
免疫抑制人群应该接受完整的下生殖道检查,并由多学科团队管理。对于有宫颈HSIL、原位腺癌或侵袭性癌病史的HIV(+)患者,应每年进行阴道穹窿的细胞学检查,对于65岁以上人群,仍需继续随访,因为仍具有较高的HPV相关疾病发生率。对于接受了子宫切除的HIV(+)人群,即便没有宫颈病变,也应长期随访。
阴道上皮内病变患者应长期随访。阴道癌前病变治疗后可能影响患者的生活质量,并增加了焦虑、抑郁等精神心理疾病的发生。专业医师应充分沟通、给予精神心理支持,以及伴侣教育,最大程度减少对患者生活质量的影响。
1.VaIN的治疗根据病变的级别高低而不同,VaIN 1(低级别阴道SIL)可以随访观察,VaIN 2/3(高级别阴道SIL)应予以治疗(共识:90%)。
2.治疗需要根据患者特性、疾病范围和既往治疗情况进行个体化进行(共识:100%)。
3.手术切除是主要的治疗方法,如果不能除外浸润性癌,应手术治疗。全阴道切除术仅用于高度选择的广泛和持续性疾病(共识:100%)。
4.CO2激光既可用作消融方法,也可用作切除方法。报道的激光切除和激光消融后的治愈率相似(共识:90%)。
5.局部药物治疗对持续性、多灶性病变或不能接受手术的患者有效(共识:95%)。
6.咪喹莫特与最低的复发率、最高的HPV清除率相关,被认为是最佳的局部药物治疗方法(共识:100%)。
7.三氯乙酸和5-氟脲嘧啶是既往选项,现不被推荐(共识:100%)。
8.对于因CIN 3子宫切除术后的VaIN,激光和局部药物不是最佳选择,因为它们不能到达埋藏在阴道瘢痕中的上皮细胞。在这些情况下,手术是首选(共识:100%)。
9.近距离放射治疗有很高的整体成功率,但由于后期副作用只用于不满足手术条件的患者,如存在多灶性病变以及既往治疗失败的患者(共识:100%)。
10.VaIN倾向于复发,确保患者坚持密切随访至关重要。首次评估应在6个月时进行,在2年内行细胞学和HPV检测,此后每年进行一次(共识:100%)。
11.实施抗HPV感染的疫苗接种可能有助于预防VaIN,从而预防阴道癌(共识:100%)。
12.治疗的效果可能会影响生活质量,并导致心理和精神问题,应予以解决(共识:100%)。
13.VaIN患者需要关于各种治疗方案清晰的和最新的资料,包括风险和获益、随访的必要性和复发风险(共识:100%)。
译者:
河北省人民医院妇科 王雅卓
河北省人民医院妇科 张迪